Диоксид кремния (:nktvn; tjybunx)
| Диоксид кремния | |
|---|---|
 | |
| | |
| Общие | |
| Систематическое наименование |
Оксид кремния(IV) |
| Традиционные названия | Диоксид кремния; кремнезём |
| Хим. формула | SiO2 |
| Внешний вид | E551 - в виде наночастиц сферической формы, размером 20–60 нм |
| Физические свойства | |
| Молярная масса | 60.0843 г/моль |
| Плотность | от 1,96 до 2,6 г/см³ |
| Удельное электрическое сопротивление | от 10¹¹ до 10¹³ Ом·м |
| Термические свойства | |
| Температура | |
| • плавления | 1710°C |
| • кипения | 2230 (4046°F) °C |
| Давление пара | 0 ± 1 мм рт.ст. |
| Классификация | |
| Рег. номер CAS | 7631-86-9 |
| PubChem | 24261 |
| Рег. номер EINECS | 231-545-4 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E551 |
| RTECS | VV7565000 |
| ChEBI | 30563 |
| ChemSpider | 22683 |
| Безопасность | |
| Предельная концентрация | 3 мг/м³ |
| ЛД50 | 3500 мг/кг |
| Токсичность | токсичен в виде наночастиц (E551, аэросил), сут. доза для чел. - 1 мг/кг |
| Пиктограммы ECB |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Диоксид кремния (кремнезём, SiO2; лат. silica) — оксид кремния (IV). Бесцветные кристаллы, практически нерастворимые в воде, обладающие высокой твёрдостью и прочностью.
Диоксид кремния — главный компонент почти всех земных горных пород, в частности, кизельгура. Из кремнезёма и силикатов состоит 87 % массы литосферы. В крови и плазме человека концентрация кремнезёма составляет 0,001 % по массе[2].
Свойства
[править | править код]- Относится к группе кислотных оксидов.
- При нагревании взаимодействует с основными оксидами и щелочами.
- Молярная масса: 60,084 г/моль
- Реагирует с плавиковой кислотой.
- SiO2 относится к группе стеклообразующих оксидов, то есть склонен к образованию переохлаждённого расплава — стекла.
- Диэлектрик (электрический ток не проводит, если не имеет примесей и не нагревается).
Полиморфизм
[править | править код]Диоксид кремния имеет несколько полиморфных модификаций.
Самая распространённая из них на поверхности земли — α-кварц — кристаллизуется в тригональной сингонии. При нормальных условиях диоксид кремния чаще всего находится в полиморфной модификации α-кварца, которая при температуре выше +573 °C обратимо переходит в β-кварц. При дальнейшем повышении температуры кварц переходит в тридимит и кристобалит. Эти полиморфные модификации устойчивы при высоких температурах и низких давлениях.
В природе также встречаются формы — опал, халцедон, кварцин, лютецит, аутигенный кварц, которые относятся к группе кремнезёма. Опал (SiO2·nH2O) в шлифе бесцветен, изотропен, имеет отрицательный рельеф, отлагается в морских водоёмах, входит в состав многих кремнистых пород. Халцедон, кварцин, лютецит — SiO2 — представляют собой скрытокристаллические разновидности кварца. Образуют волокнистые агрегаты, розетки, сферолиты, бесцветные, голубоватые, желтоватые. Отличаются между собой некоторыми свойствами — у халцедона и кварцина — прямое погасание, у лютецита — косое, у халцедона — отрицательное удлинение.
При высоких температуре и давлении диоксид кремния сначала превращается в коэсит (который в 1953 году был синтезирован американским химиком Лорингом Коэсом), а затем — в стишовит (который в 1961 году был синтезирован С. М. Стишовым, а в 1962 году был обнаружен в кратере Бэрринджера (кратере Аризонского метеорита)[3][4]. Согласно некоторым исследованиям[каким?], стишовит слагает значительную часть мантии, так что вопрос о том, какая разновидность SiO2 наиболее распространена на Земле, пока не имеет однозначного ответа.[источник не указан 1637 дней]
Также имеет аморфную модификацию — кварцевое стекло.
Химические свойства
[править | править код]Диоксид кремния SiO2 — кислотный оксид, не реагирующий с водой.
Химически стоек к действию кислот, но реагирует с газообразным фтороводородом:
Эти две реакции широко используют для травления стекла.
При сплавлении SiO2 с щелочами и основными оксидами, а также с карбонатами активных металлов образуются силикаты — соли не имеющих постоянного состава очень слабых, нерастворимых в воде кремниевых кислот общей формулы xH2O·ySiO2 (довольно часто в литературе упоминаются не кремниевые кислоты, а кремниевая кислота, хотя фактически речь при этом идёт об одном и том же веществе).
Например, может быть получен ортосиликат натрия:
или смешанный силикат кальция и натрия:
Из силиката Na2CaSi6O14 (Na2O·CaO·6SiO2) изготовляют оконное стекло.
Большинство силикатов не имеет постоянного состава. Из всех силикатов растворимы в воде только силикаты натрия и калия. Растворы этих силикатов в воде называют жидким стеклом. Из-за гидролиза эти растворы характеризуются сильно щелочной средой. Для гидролизованных силикатов характерно образование не истинных, а коллоидных растворов. При подкислении растворов силикатов натрия или калия выпадает студенистый белый осадок гидратированных кремниевых кислот.
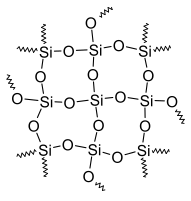
Главным структурным элементом как твёрдого диоксида кремния, так и всех силикатов, выступает группа [SiO4/2], в которой атом кремния Si окружен тетраэдром из четырёх атомов кислорода О. При этом каждый атом кислорода соединён с двумя атомами кремния. Фрагменты [SiO4/2] могут быть связаны между собой по-разному. Среди силикатов по характеру связи в них фрагментов [SiO4/2] выделяют островные, цепочечные, ленточные, слоистые, каркасные и другие.
При особых условиях взаимодействует с водой.
Окислительные свойства не характерны, и проявляются лишь в реакциях с сильными восстановителями: углём, алюминием, магнием, кальцием.
Получение
[править | править код]Синтетический диоксид кремния получают нагреванием кремния до температуры +400…+500 °C в атмосфере кислорода, при этом кремний окисляется до диоксида SiO2. А также термическим оксидированием при больших температурах.
В лабораторных условиях синтетический диоксид кремния может быть получен действием кислот, даже слабой уксусной, на растворимые силикаты. Например:
кремниевая кислота сразу распадается на воду и SiO2, выпадающий в осадок.
Натуральный диоксид кремния в виде песка используется там, где не требуется высокая чистота материала.
Применение
[править | править код]В разделе не хватает ссылок на источники (см. рекомендации по поиску). |
Аморфный непористый диоксид кремния применяется в пищевой промышленности в качестве вспомогательного вещества E551, препятствующего слёживанию и комкованию, в парафармацевтике (зубные пасты), в фармацевтической промышленности в качестве вспомогательного вещества (внесён в большинство фармакопей), для стабилизации суспензий и линиментов, в качестве загустителя мазевых основ, наполнителя таблеток и суппозиториев. Он входит в состав композиции пломбировочных материалов, снижает гигроскопичность сухих экстрактов, замедляет выход БАВ из различных лекарственных форм; в качестве пищевых добавок и сорбента, а также матриц для создания лекарственных форм с заданными свойствами — так как нет кристаллической структуры (аморфен)[5], а также в качестве пищевой добавки или лекарственного препарата в качестве энтеросорбента Полисорб МП с широким спектром применения с учётом высокой удельной поверхности сорбции (в интервале 300—400 м²) на 1 г основного вещества.
Диоксид кремния применяют в производстве стекла, керамики, абразивов, бетонных изделий, для получения кремния, как наполнитель в производстве резин, при производстве кремнезёмистых огнеупоров, в хроматографии и другом.
Кристаллы кварца обладают пьезоэлектрическими свойствами и поэтому используются в радиотехнике, ультразвуковых установках, в зажигалках, в изготовлении оргонитов.
Также используется для производства волоконно-оптических кабелей. Используется чистый плавленый диоксид кремния с добавкой в него некоторых специальных ингредиентов.
Кремнезёмная нить также используется в нагревательных элементах электронных сигарет, так как хорошо впитывает жидкость и не разрушается под нагревом спирали.
Также диоксид кремния нашёл наиболее широкое применение в шинной промышленности, производстве РТИ и пластмасс, химической промышленности, машиностроении, а в ряде конкретных операций:
- как носитель катализаторов и химических средств защиты растений;
- в качестве сорбентов и фильтровальных порошков для регенерации нефтепродуктов;
- как высококачественный флюс в процессах цветной металлургии;
- как сырьё для производства экологически чистого стекла, стеклотары и хрусталя;
- как наполнитель в бумагу и картон для получения гигиенически чистых упаковочных материалов для пищевой промышленности;
- фильтрующие порошки для пива, масел, соков, матирующие добавки в лаки и краски;
- для получения карбида кремния в машиностроении — керамические двигатели, детали для авиастроительного комплекса;
- для получения кристаллического кремния в электронной и электротехнической промышленностях, керамические электроизоляторы, стекловолокна, волоконная оптика, супертонкое волокно;
- для синтеза искусственных цеолитов в нефтехимии — крекинг нефти и прочее.
Крупные прозрачные кристаллы кварца используются в качестве полудрагоценных камней; бесцветные кристаллы называют горным хрусталём, фиолетовые — аметистами, жёлтые — цитрином.
В микроэлектронике диоксид кремния является одним из основных материалов. Его применяют в качестве изолирующего слоя (например, подзатворного диэлектрика в полевых транзисторах), а также в качестве защитного покрытия. Получают в виде тонких плёнок термическим окислением кремния, химическим осаждением из газовой фазы, магнетронным распылением.
Пористые кремнезёмы
[править | править код]Пористые кремнезёмы получают различными методами.
Силохром получают путём агрегирования аэросила, который, в свою очередь, получают сжиганием силана (SiH4). Силохром характеризуется высокой чистотой, низкой механической прочностью. Характерный размер удельной поверхности 60—120 м²/г. Применяется в качестве сорбента в хроматографии, наполнителя резин, катализе.
Силикагель получают путём высушивания геля кремниевой кислоты. В сравнении с силохромом обладает меньшей чистотой, однако может обладать чрезвычайно развитой поверхностью: обычно от 300 м²/г до 700 м²/г .
Кремниевый аэрогель приблизительно на 99,8 % состоит из воздуха и может иметь плотность до 1,9 кг/м³ (всего в 1,5 раза больше плотности воздуха).
Так же существует современный и экологичный способ получения диоксида кремния из рисовой лузги и отходов сельскохозяйственных производств.
Токсичность
[править | править код]В виде наночастиц
Способность наночастиц проникать через биологические барьеры и накапливаться в организме, их высокая химическая и каталитическая активность, определяют наличие у многих наночастиц токсических свойств, которые необходимо учитывать при оценке возможных рисков их воздействия на человека. В качестве основных критериев рисков наночастиц используются объем их производства и неспособность к растворению в воде и биологических средах.[6]
Согласно ТР ТС 021/20111 пищевая продукция, содержащая наночастицы или произведённая с использованием нанотехнологий и обладающая свойствами, рассматривается как «продукция нового вида», для которой обязательной является оценка соответствия в форме государственной регистрации.[6]
К 2018 году в России и Таможенном союзе прошли государственную регистрацию в качестве пищевой продукции нового вида около 60 видов продукции наноиндустрии. В основном это биологически активные добавки к пище (БАД), содержащие пищевые вещества в наноформе, комплексные пищевые добавки – эмульгаторы и отдельные виды технологических вспомогательных средств и композитных упаковочных материалов, использующих наноглины. Однако, анализ ассортимента представленной на рынке пищевой продукции, нормативно-правовых документов, устанавливающих требования к ее составу и безопасности, показывает, что масштабы использования пищевых добавок в виде наночастиц и наноматериалов в пищевых производствах, возможно, недооценены, поскольку размер частиц не регулируется и не конролируется ни российской, ни международной нормативной базой, особенно диоксид кремния аморфный и диоксид титана.[6]
Диоксид кремния в виде Е551 применяется в качестве антислеживающего агента и носителя. ТР ТС 029/20122 устанавливает допустимые уровни его содержания в пряностях (не более 30 г/кг), продуктах, плотно обернутых фольгой (30 г/кг), сахарной пудре (10 г/кг), соли и ее заменителях (10 г/кг), сырах и сырных продуктах (10 г/кг), ароматизаторах (50 г/кг). Использование пищевого сырья, содержащего Е551, допускается при производстве продуктов для питания детей. В таблетированной пищевой продукции, БАД к пище, сахаристых кондитерских изделиях (кроме шоколада) содержание Е551 не регламентируется. Помимо указанной пищевой продукции, поступление аморфного SiO2 возможно с фармацевтическими препаратами и косметической продукцией (зубные пасты и др.).[6] В общем объеме Е551 значительную долю составляет такая ее форма, как высокодисперсный пирогенный SiO₂ («Аэросил»), имеющий удельную площадь поверхности 300–380 м²/г, в виде наночастиц сферической формы и размером около 20–60 нм, которые образованы на ультраструктурном уровне слабо связанными (агломерированными).[6]
Однако в спецификации JECFA на данную пищевую добавку отсутствует информация о размере ее частиц, который, как правило, не контролируется и не декларируется производителями продукции, вследствие чего значительный объем пищевой продукции, находящейся в обороте, может содержать данное вещество в форме наноматериала, а по некоторым данным пищевая экспозиция человека наночастицами SiO2 может превышать в настоящее время 1,8 мг/кг массы тела в сутки. В исследованиях на лабораторных животных наночастицы SiO2 были биодоступны при поступлении в желудочно-кишечный тракт, а в 3-х месячном подостром эксперименте при дозе наноразмерного SiO2 типа «Аэросил» 100 мг/кг массы тела у животных наблюдалась лейкопения, снижалась доля Т-хелперов, возрастала доля цитотоксических лимфоцитов, снижался иммунорегуляторный индекс (CD4/CD8), отмечался дисбаланс про- и противовоспалительных цитокинов, что в совокупности означает неблагоприятное воздействие на систему иммунитета. Морфологическое исследование показало, что мишенью воздействия поступающих с пищей наночастиц SiO2 является слизистая оболочка тонкой кишки, где наблюдается массивная лимфомакрофагальная и эозинофильная инфильтрации ворсинок.[6]
С учетом введения двух 10-кратных коэффициентов запаса при переносе данных, полученных в in vivo модели, на человека возможная допустимая суточная дозы наночастиц SiO₂, поступающих с пищей, составляет не более 1 мг/кг массы тела.[6]
- Ранее считалось, что вещество малотоксично: ПДК в рабочей зоне - 3 мг/м³. ЛД50 на крысах - 3500 мг/кг. (источник?)
- При попадании кристаллического диоксида кремния в ткани организма происходит возникновение и постепенное развитие гранулом.
- При вдыхании пыли кристаллического диоксида кремния происходит раздражение дыхательных путей, также возникают различные заболевания пищевого тракта. Постоянное воздействие пыли может вызвать силикоз лёгких[2]. Аморфная структура является безвредной.
Примечания
[править | править код]- ↑ PubChem Hazardous Substances Data Bank (HSDB) : 7168 (англ.). pubchem.ncbi.nlm.nih.gov. Дата обращения: 30 октября 2024.
- ↑ 1 2 Сахаров, 1990.
- ↑ Справочник химика 21 — Стишовит. Дата обращения: 23 сентября 2019. Архивировано 23 сентября 2019 года.
- ↑ Лисичкин Г. В. Химия привитых поверхностных соединений. Дата обращения: 23 сентября 2019. Архивировано 19 июня 2017 года.
- ↑ Медицинская химия и клиническое применение диоксида кремния : моногр. / [А. А. Чуйко, В. А. Тертых, В. В. Лобанов и др.] ; Под ред. А. А. Чуйко ; Нац. акад. наук Украины. Ин-т химии поверхности. — Киев : Наукова думка, 2003. — 414, [1] с. : ил., табл. — ISBN 966-00-0185-1.
- ↑ 1 2 3 4 5 6 7 Гмошинский И.в, Шипелин В.а, Хотимченко С.а. Наноматериалы в пищевой продукции и ее упаковке: сравнительный анализ рисков и преимуществ // Анализ риска здоровью. — 2018. — Вып. 4. — С. 134–142. — ISSN 2308-1155. Архивировано 4 сентября 2022 года.
Литература
[править | править код]- И. Е. Неймарк // Силикагель, его получение, свойства и применение. 1973 — Киев — 200 с.
- Сахаров В. В. Кремния диоксид // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Советская энциклопедия, 1990. — Т. 2: Даффа — Меди. — С. 517—518. — 671 с. — 100 000 экз. — ISBN 5-85270-035-5.
- А. И. Врублевский //Основы химии


![{\displaystyle {\mathsf {SiO_{2}+6HF\rightarrow H_{2}[SiF_{6}]+2H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/13b99cb061378a488154c85d2b6585eaba673596)



