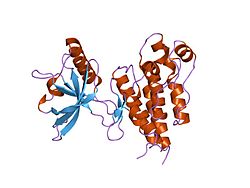
KDR (KDR)
KDR (англ. Kinase insert domain receptor, CD309), или Рецептор фактора роста сосудистого эндотелия, тип 2 (англ. vascular endothelial growth factor receptor 2, VEGFR-2), — белок тирозинкиназа, рецептор фактора роста VEGF, продукт гена человека KDR.
Функции
[править | править код]Протеинкиназа VEGFR-2 действует как рецептор для факторов роста VEGFA, VEGFC и VEGFD. Играет важную роль в регуляции ангиогенеза, сосудистого развития, проницаемости сосудов и эмбрионального гематопоэза. Повышает пролиферацию, выживаемость, миграцию и дифференцировку эндотелиальных клеток. Приводит к реорганизации актинового цитоскелета клетки. Изоформы 2 и 3, у которых отсутствует трансмембранный домен, могут действовать как ингибирующие рецепторы для факторов роста VEGFA, VEGFC и VEGFD. Изоформа 2 действует как отрицательный регулятор лимфангиогенеза, опосредованного VEGFA и VEGFC, за счёт ограничения количества свободных VEGFA и/или VEGFC и предотвращения их связывания с FLT4.
Модулирует сигнальнуе пути FLT1 и FLT4, образуя гетеродимеры с последними. Связывание VEGF с изоформой 1 VEGFR-2 приводит к активации нескольких сигнальных путей. Активация PLCG1 приводит к генерации таких вторичных посредников как диацилглицерина и 1,4,5-трифосфата и активации протеинкиназы C. Опосредует активацию сигнальных путей MAPK1/ERK2, MAPK3/ERK1 и the MAP-киназ, а также AKT1. Опосредует фосфорилирование регуляторной субъединицы фосфатидилинозитол-3-киназы PIK3R1. VEGFR-2 способен индуцировать NOS2 и NOS3, что приводит к синтезу окиси азота (NO) эндотелиальными клетками
Фофорилирует PLCG1, а также может фосфорилировать FYN, NCK1, NOS3, PIK3R1, PTK2/FAK1 и SRC[5][6].
Взаимодействия
[править | править код]VEGFR-2 взаимодействует с SHC2,[7] Аннексин A5[8] и SHC1.[9][10]
См. также
[править | править код]Литература
[править | править код]- Holmes K., Roberts O.L., Thomas A.M., Cross M.J. Vascular endothelial growth factor receptor-2: structure, function, intracellular signalling and therapeutic inhibition (англ.) // Cellular Signalling[англ.] : journal. — 2007. — October (vol. 19, no. 10). — P. 2003—2012. — doi:10.1016/j.cellsig.2007.05.013. — PMID 17658244.
- Petrova T.V., Makinen T., Alitalo K. Signaling via vascular endothelial growth factor receptors (англ.) // Experimental Cell Research[англ.] : journal. — 1999. — November (vol. 253, no. 1). — P. 117—130. — doi:10.1006/excr.1999.4707. — PMID 10579917.
- Wang J., Fu X., Jiang C., Yu L., Wang M., Han W., Liu L., Wang J. Bone marrow mononuclear cell transplantation promotes therapeutic angiogenesis via upregulation of the VEGF-VEGFR2 signaling pathway in a rat model of vascular dementia (англ.) // Behavioural Brain Research[англ.] : journal. — 2014. — May (vol. 265). — P. 171—180. — doi:10.1016/j.bbr.2014.02.033. — PMID 24589546. — PMC 4000455.
- Sato Y., Kanno S., Oda N., Abe M., Ito M., Shitara K., Shibuya M. Properties of two VEGF receptors, Flt-1 and KDR, in signal transduction (англ.) // Annals of the New York Academy of Sciences[англ.] : journal. — 2000. — May (vol. 902, no. 1). — P. 201—205. — doi:10.1111/j.1749-6632.2000.tb06314.x. — . — PMID 10865839.
- Zachary I., Gliki G. Signaling transduction mechanisms mediating biological actions of the vascular endothelial growth factor family (англ.) // Cardiovascular Research[англ.] : journal. — 2001. — February (vol. 49, no. 3). — P. 568—581. — doi:10.1016/S0008-6363(00)00268-6. — PMID 11166270.
- Vené R., Benelli R., Noonan D.M., Albini A. HIV-Tat dependent chemotaxis and invasion, key aspects of tat mediated pathogenesis (англ.) // Clinical & Experimental Metastasis : journal. — 2001. — Vol. 18, no. 7. — P. 533—538. — doi:10.1023/A:1011991906685. — PMID 11688957.
- Lenton K. VEGFR-2 (KDR/Flk-1) (англ.) // Journal of Biological Regulators and Homeostatic Agents[нем.]. — 2003. — Vol. 16, no. 3. — P. 227—232. — PMID 12456025.
- Matsumoto T., Mugishima H. Signal transduction via vascular endothelial growth factor (VEGF) receptors and their roles in atherogenesis (англ.) // Journal of Atherosclerosis and Thrombosis : journal. — 2006. — June (vol. 13, no. 3). — P. 130—135. — doi:10.5551/jat.13.130. — PMID 16835467.
Примечания
[править | править код]- ↑ 1 2 3 GRCh38: Ensembl release 89: ENSG00000128052 - Ensembl, May 2017
- ↑ 1 2 3 GRCm38: Ensembl release 89: ENSMUSG00000062960 - Ensembl, May 2017
- ↑ Ссылка на публикацию человека на PubMed: Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ↑ Ссылка на публикацию мыши на PubMed: Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ↑ Simons M., Gordon E., Claesson-Welsh L. Mechanisms and regulation of endothelial VEGF receptor signalling. (англ.) // Nat Rev Mol Cell Biol : journal. — 2016. — Vol. 17, no. 10. — P. 611—625. — doi:10.1038/nrm.2016.87. — PMID 27461391.
- ↑ Zafar M.I., Zheng J., Kong W., Ye X., Gou L., Regmi A et al. The role of vascular endothelial growth factor-B in metabolic homoeostasis: current evidence. (англ.) // Biosci Rep : journal. — 2017. — Vol. 37, no. 4. — doi:10.1042/BSR20171089. — PMID 28798193. — PMC 5577206.
- ↑ Warner A.J., Lopez-Dee J., Knight E.L., Feramisco J.R., Prigent S.A. The Shc-related adaptor protein, Sck, forms a complex with the vascular-endothelial-growth-factor receptor KDR in transfected cells (англ.) // The Biochemical Journal[англ.] : journal. — 2000. — April (vol. 347, no. Pt 2). — P. 501—509. — doi:10.1042/0264-6021:3470501. — PMID 10749680. — PMC 1220983.
- ↑ Wen Y., Edelman J.L., Kang T., Sachs G. Lipocortin V may function as a signaling protein for vascular endothelial growth factor receptor-2/Flk-1 (англ.) // Biochemical and Biophysical Research Communications : journal. — 1999. — May (vol. 258, no. 3). — P. 713—721. — doi:10.1006/bbrc.1999.0678. — PMID 10329451.
- ↑ Zanetti A., Lampugnani M.G., Balconi G., Breviario F., Corada M., Lanfrancone L., Dejana E. Vascular endothelial growth factor induces SHC association with vascular endothelial cadherin: a potential feedback mechanism to control vascular endothelial growth factor receptor-2 signaling (англ.) // Arteriosclerosis, Thrombosis, and Vascular Biology[англ.] : journal. — 2002. — April (vol. 22, no. 4). — P. 617—622. — doi:10.1161/01.ATV.0000012268.84961.AD. — PMID 11950700.
- ↑ D'Angelo G., Martini J.F., Iiri T., Fantl W.J., Martial J., Weiner R.I. 16K human prolactin inhibits vascular endothelial growth factor-induced activation of Ras in capillary endothelial cells (англ.) // Molecular Endocrinology[англ.] : journal. — 1999. — May (vol. 13, no. 5). — P. 692—704. — doi:10.1210/mend.13.5.0280. — PMID 10319320.