Диены (:nyud)
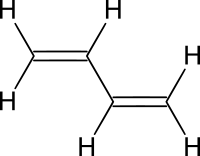
Алкадие́ны (дие́ны, дие́новые углеводоро́ды, диолефи́ны) — ациклические непредельные углеводороды, содержащие две двойных связи углерод-углерод, образующие гомологический ряд с общей формулой CnH2n-2.[1][2]
Атомы углерода при двойных связях находятся в состоянии sp-гибридизации. Простейшим алкадиеном является пропадиен (C3H4), относящийся к кумулированным диенам.
По номенклатуре «IUPAC», названия алкадиенов образуются от названий соответствующих алканов заменой суффикса «-ан» на «-дие́н». Положение двойных связей указывается арабской цифрой.
Классификация
[править | править код]В зависимости от взаимного расположения кратных связей, диены подразделяются на три группы[1]:
1) Диены с алле́новыми (кумули́рованными) связями (1,2-диены): CH2=С=CH2;
2) Диены с сопряжёнными связями: двойные связи разделены одной одинарной связью (1,3-диены): СH2=CH−CH=CH2;
3) Диены с изоли́рованными связями: двойные связи разделены более, чем одной одинарной: CH2=CH−(CH2)n−CH=CH2, где n ≥ 1;
Гетероаналоги диенов, в которых один из ненасыщенных углеродных атомов замещён гетероатомом, называются гетеродиенами.[1]
Обычно к диенам относят ациклические и циклические 1,3-диены, образующие гомологические ряды общих формул и соответственно, ациклические диены являются структурными изомерами алкинов.
Гомологический ряд
[править | править код]Гомологический ряд алкадиенов:
| Название диена | Химическая формула |
| Пропадиен | C3H4 |
| Бутадиен (дивинил) | C4H6 |
| Пентадиен-1,3 (пиперилен) | C5H8 |
| Гексадиен | C6H10 |
| Гептадиен | C7H12 |
| Октадиен | C8H14 |
| Нонадиен | C9H16 |
| Декадиен | C10H18 |
Физические свойства
[править | править код]Низшие диены — бесцветные легкокипящие жидкости (температура кипения изопрена 34 °C; температура кипения 2,3-диметил-1,3-бутадиена 68,78 °C; температура кипения 1,3-циклопентадиена 41,5 °C). 1,3-Бутадиен и аллен (1,2-пропадиен) — газы (Tкип −4,5 °C и −34 °C соответственно).
Сопряжённые диены существуют в виде двух конформаций — цисоидной (s-цис-форма) и трансоидной (s-транс-форма), способных переходить друг в друга, более устойчивой является s-транс-форма:
Химические свойства
[править | править код]Реакционная способность диенов определяется спецификой сопряжения двойных связей — если для диенов с изолированными двойными связями реакционная способность аналогична реакционной способности алкенов, то в случае алленов и 1,3-диенов эффекты сопряжения ведут к специфике реакционной способности этих классов соединений.
Реакции алленов
[править | править код]Центральный sp-гибридизованный атом углерода в алленах является электрофильным центром, поэтому, в отличие от не активированных электронакцепторными заместителями алкенов, аллены реагируют с мягкими нуклеофилами, образуя винильные и аллильные производные:
Электрофильность sp-гибридизованного атома алленов повышается электроноакцепторными группами, в этом случае присоединение нуклеофила идёт исключительно по этому атому:
Гидратации аллена в условиях кислотного катализа присоединение протона идёт по терминальному углероду, образующийся при этом енол далее таутомеризуется в ацетон:
Под действием щелочей или кислот аллены могут претерпевать прототропные перегруппировки в 1,3-диены:
Реакции 1,3-диенов
[править | править код]Специфика реакционной способности 1,3-диенов обусловлена мезомерией вследствие сопряжения двойных связей:
Результатом является то, что в случае электрофильного присоединения к сопряжённым диенам типичны реакции 1,4-присоединения, идущие через промежуточное образование резонансно стабилизированных аллильных карбокатионов:
- ,
где Х — это Hal, H, а Y — это Hal, OH
Сопряжённые диены легко полимеризуются по механизму 1,4-присоединения, реакция полимеризации 1,3-диенов лежат в основе синтеза диеновых каучуков.
Диены также реагируют с алкенами и другими соединениями — диенофилами с активированной электронакцепторными заместителями кратной связью, образуя продукты [4+2]-присоединения (реакция Дильса — Альдера)
Получение
[править | править код]Формально эту реакцию можно представить как дегидратацию двух молекул этилового спирта с одновременным межмолекулярным дегидрированием.
См. также
[править | править код]Примечания
[править | править код]- ↑ 1 2 3 The International Union of Pure and Applied Chemistry (IUPAC). Определение диенов по номенклатуре ИЮПАК. goldbook.iupac.org. Дата обращения: 26 марта 2023. Архивировано 29 марта 2023 года.
- ↑ Степаненко Б. Н. Органическая химия. — 4-е изд., перераб. — М.: Медицина, 1970. — С. 44, 50—51. — 336 с.
Литература
[править | править код]- Грандберг И.И., Нам Н.Л. Органическая химия. Учебник для СПО. — 8-е изд. — Москва: Юрайт, 2016. — 608 с. — ISBN 978-5-9916-6328-1.
- Каминский В.А. Органическая химия. В 2 ч. Часть 1. — 2-е изд. — Москва: Юрайт, 2019. — 287 с. — ISBN 978-5-534-02906-2.
В статье не хватает ссылок на источники (см. рекомендации по поиску). |





![{\displaystyle {\mathsf {CH_{2}\!\!=\!\!C\!\!=\!\!CH_{2}+H_{2}O}}\rightarrow {\mathsf {[CH_{2}\!\!=\!\!C(OH)CH_{3}]}}\rightarrow {\mathsf {CH_{3}COCH_{3}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e52f821e650c4a6ac6bfd9ab7dbdce3f56191aa8)






