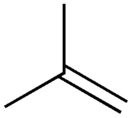
Изобутилен (N[kQrmnlyu)

| Изобутилен | |||
|---|---|---|---|
| |||
| Общие | |||
| Хим. формула | C4H8 | ||
| Физические свойства | |||
| Молярная масса | 56.11 г/моль | ||
| Плотность | 0.5879 г/см³ | ||
| Энергия ионизации | 9,24 эВ[1] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | −140,4 °C[1] | ||
| • кипения | -6.9 °C | ||
| Критическая точка | |||
| • температура | 144,73 °C | ||
| • давление | 39,48 атм | ||
| Структура | |||
| Дипольный момент | 1,7E−30 Кл·м[1] | ||
| Классификация | |||
| Рег. номер CAS | 115-11-7 | ||
| PubChem | 8255 | ||
| Рег. номер EINECS | 204-066-3 | ||
| SMILES | |||
| InChI | |||
| RTECS | UD0890000 | ||
| ChEBI | 43907 | ||
| Номер ООН | 1055 | ||
| ChemSpider | 7957 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Изобутилен (СН3)2С=СН2 — ненасыщенный углеводород, изомерен бутилену.
Нахождение в природе
[править | править код]Содержится в газах крекинга нефти.
Получение
[править | править код]Изобутилен в промышленности получают выделением из бутан-бутеновой фракции производства бензинов или этилена каталитическим или термическим крекингом или пиролизом жидких нефтепродуктов или нефтяных газов[2]. Выход фракции С4 в этих трех процессах составляет соответственно 3-10, 1-2 и 0,4-5 мас.%. Изобутилен из фракций C4 выделяют путём экстракции 65%-ной серной кислотой (способ А.М. Бутлерова) при температурах, близких к комнатной. Экстракция протекает практически количественно. Итогом процесса является трет-бутилсерная кислота
(CH3)2C=CH2 + H2SO4 = (CH3)3COSO3H
которую вновь превращают в изобутилен.
Другой способ состоит в выделении его из бутилсерной кислоты гидролизом её острым паром, в результате чего образуется трет-бутиловый спирт.
(CH3)3COSO3H + H2O = (CH3)3COH + H2SO4
Последний дегидратируют 30%-ной серной кислотой до получения изобутилена. Однако применение этого способа ограничено высокой стоимостью процесса регенерации серной кислоты.
Более эффективен способ, в котором реакционную жидкость, полученную экстракцией изобутилена 65%-ной кислотой, разбавляют водой до концентрации кислоты 45%. При нагревании этого раствора при низком давлении выделяется чистым изобутилен, который промывают щелочью, освобождают от спирта путём охлаждения, промывают водой и сжижают под давлением.
Фирма Union Carbide разработала процесс выделения изобутена из бутан-бутиленовой фракции путём адсорбции на цеолитах. В этом процессе также выделяют бутилен, который изомеризуют в изобутилен.
Другим способом получения изобутилена является каталитическое дегидрирование изобутана.
Применение
[править | править код]Применяется для получения изооктана, метакролеина, синтетических смол. Реакцией со спиртами могут быть получены простые трет-бутиловые эфиры (МТБЭ, ЭТБЭ и др.), применяемые в качестве добавок к моторному топливу.
Присоединение формальдегида к изобутилену с последующей дегидратацией является одним из промышленных методов синтеза изопрена, использующегося в производстве синтетических каучуков:
Примечания
[править | править код]- ↑ 1 2 3 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ Н.А.Платэ, Е.В.Сливинский. Основые химии и технологии мономеров. — Москва: «Наука», МАИК «Наука/Интерпериодика», 2002. — 696 с. — ISBN 5-02-006396-7.
Это заготовка статьи об органическом веществе. Помогите Википедии, дополнив её. |
В статье не хватает ссылок на источники (см. рекомендации по поиску). |