Мимивирус (Bnbnfnjrv)
Информация в этой статье или некоторых её разделах устарела. |
| Мимивирус | ||||||||
|---|---|---|---|---|---|---|---|---|
![Мимивирус под электронным микроскопом[1]](http://upload.wikimedia.org/wikipedia/commons/thumb/5/57/Electron_microscopic_image_of_a_mimivirus_-_journal.ppat.1000087.g007_crop.png/275px-Electron_microscopic_image_of_a_mimivirus_-_journal.ppat.1000087.g007_crop.png) Мимивирус под электронным микроскопом[1] | ||||||||
| Научная классификация | ||||||||
|
Реалм: Царство: Класс: Порядок: Imitervirales Семейство: Род: Мимивирус |
||||||||
| Международное научное название | ||||||||
| Mimivirus | ||||||||
| Группа по Балтимору | ||||||||
| I: дцДНК-вирусы | ||||||||
| ||||||||
Мимивирус[3] (лат. Mimivirus) — род вирусов, включающий в себя единственный вид Acanthamoeba polyphaga mimivirus (APMV), хозяевами которого являются амёбы рода Acanthamoeba.
До октября 2011 года, когда был описан ещё более крупный Megavirus chilensis[4][5], считалось, что мимивирус обладает самым крупным капсидом среди всех известных вирусов — около 500 нм в диаметре[6]. В отличие от большинства других вирусов, мимивирус не проходит через фильтр с диаметром пор 0,22 мкм и виден в световой микроскоп, по размерам он близок к небольшим бактериям, таким как микоплазма[7]. Кроме того, по сравнению с другими вирусами и даже некоторыми бактериями, мимивирус обладает более объёмным (около 1,2 миллионов пар нуклеотидов) и сложноструктурированным геномом[8][9].
В свете нехватки точных данных о природе данного вируса его открытие вызвало большой интерес в научных кругах. Один из первооткрывателей мимивируса высказал предположение, что он представляет собой недостающее звено между вирусами и клеточными организмами[10]. Имеется и более радикальное мнение, согласно которому мимивирус представляет собой принципиально новую форму жизни, не относящуюся к вирусам или бактериям[11].
Этимология названия
[править | править код]Название «мимивирус» было дано этому вирусу как сокращение от «мимикрирующий под микроб» (англ. mimicking microbe virus). Это связано с тем, что некоторое время этот вирус считали микроорганизмом, а не вирусом, на основании таких признаков, как крупный размер, наличие белковых нитей, похожих на жгутики, и способность окрашиваться по методу Грама[12].
Открытие
[править | править код]APMV был впервые обнаружен в 1992 году в амёбе Acanthamoeba polyphaga[13], в честь которой он и был назван, в ходе поисков возбудителей легионеллёза. Вирус был обнаружен в препарате, окрашенном по методу Грама, и вследствие этого ошибочно принят за грамположительную бактерию. Организм был назван Bradfordcoccus в честь района, в котором была найдена амёба (Брадфорд, Англия). После неудачных попыток культивирования и ПЦР-типирования этого организма с помощью универсальных праймеров, узнающих гены бактериальной 16S рРНК, образец пролежал в холодильнике 10 лет[10]. Позднее он был передан во Францию, где были проведены дополнительные исследования, позволившие заключить, что Bradfordcoccus на самом деле является гигантским вирусом. Результаты работы были опубликованы в 2003 году в журнале «Science»[14].
Классификация
[править | править код]Род мимивирус принадлежит к семейству Mimiviridae. Это семейство относят к внесистематической группе крупных ядерно-цитоплазматических ДНК-содержащих вирусов (англ. nucleocytoplasmic large DNA viruses, NCLDVs), к которой также относятся поксвирусы, иридовирусы, асковирусы[англ.], асфарвирусы[англ.] и фикоднавирусы[англ.][15]. Все эти вирусы отличаются крупными размерами, схожими молекулярными характеристиками и сложными геномами[14]. Ряд белков мимивируса, принимающих участие в репликации генома, оказались гомологичными белкам других крупных ядерно-цитоплазматических ДНК-содержащих вирусов, что говорит об их общем происхождении. Однако большое количество мимивирусных белков не обнаруживают сходства ни с одним известным в настоящее время белком. Кроме того, геном мимивируса кодирует значительное количество белков, напоминающих эукариотические и бактериальные. По-видимому, эти гены были приобретены мимивирусом вторично и происходят из геномов хозяев вируса и их паразитов[16].
Семейство Mimiviridae до сих пор не было отнесено Международным комитетом по таксономии вирусов (ICTV) к какому-либо отряду[17]. В 2012 году было высказано предложение сгруппировать это и несколько других семейств крупных вирусов в новый отряд Megavirales[15].
В научной литературе в последние годы можно встретить альтернативный термин, обозначающий группу гигантских вирусов — гирус[англ.][18].
Согласно классификации вирусов по Балтимору мимивирус относится к группе I (вирусы, содержащие двуцепочечную ДНК и не имеющие обратной транскриптазы). В эту группу входят такие семейства вирусов, как иридовирусы, поксвирусы и другие.
Структура
[править | править код]Капсид и внешние оболочки
[править | править код]

Мимивирус имеет примерно икосаэдрический капсид диаметром 400—500 нм[14][20]. Капсид покрыт многочисленными белковыми нитями длиной 80—120 нм. В научной литературе приводятся размеры вириона от 400 до 800 нм, в зависимости от того, замеряется ли диаметр капсида или общая длина вируса вдоль продольной оси, включая белковые нити. Основной белок капсида мимивируса является продуктом гена L425 и состоит из двух доменов с укладкой типа jelly-roll («рулет»). Этот белок формирует гомотримерные капсомеры — единицы организации капсида. Капсомеры упакованы гексагонально в виде «ромашек»: шесть капсомеров окружают одно углубление между ними[19]. Также в составе капсида обнаруживается структурный белок сердцевины L410[10].
На одной из вершин капсида обнаружена звёздчатая структура, лучи которой разделяют пять треугольных граней, сходящихся в этой вершине. Лучи имеют ширину около 50 нм, толщину — 40 нм и длину — 200 нм, почти доходя до соседних вершин. Присутствие этой структуры изменяет взаимное расположение граней вириона, в результате чего его форма отклоняется от идеально икосаэдрической: через вирион можно провести только одну ось пятилучевой симметрии, которая проходит через вершину, отмеченную звёздчатой структурой. Так как на поверхности звёздчатой структуры не наблюдается гексагонально упорядоченных углублений, предполагают, что она состоит из белка, который отличается от основного белка капсида[19]. Данная структура играет особую роль при заражении клетки-хозяина: при инфицировании звёздчатая «застёжка» открывается, и через это место ДНК вируса выходит из капсида. По этой причине звёздчатую структуру ещё называют «звёздными вратами»[21].
У мимивируса не наблюдается внешней оболочки, что указывает на то, что он покидает заражённую клетку не путём экзоцитоза[22].
Капсид мимивируса покрыт снаружи густым слоем длинных белковых нитей. Исследование этих нитей с помощью атомно-силового микроскопа показало, что они часто бывают присоединены к общей несущей структуре и заканчиваются небольшой глобулой. Однако до сих пор неизвестно, к каким участкам поверхности капсида они прикрепляются[19]. Белковые нити устойчивы к воздействию протеаз до тех пор, пока их не обработать лизоцимом, это указывает на то, что эти нити покрыты пептидогликаном. Это хорошо согласуется с тем, что мимивирус окрашивается по методу Грама. Существует мнение, что сильно гликозилированная поверхность нитей может играть роль в привлечении амёб-хозяев[20].
Нуклеокапсид
[править | править код]Мимивирус обладает многими особенностями строения, характерными для других крупных ядерно-цитоплазматических ДНК-содержащих вирусов. Например, сразу под капсидом у мимивируса находятся два электронноплотных слоя, которые предположительно являются мембранами[20]. Под этими мембранами находится белковая оболочка толщиной около 7 нм, внутри которой заключена линейная двухцепочечная ДНК вируса. Все описанные компоненты образуют так называемый нуклеокапсид. Стенки нуклеокапсида отстают от стенок капсида примерно на 30 нм, в районе звёздчатой структуры поверхность нуклеокапсида вдавлена[19]. Предполагают, что пространство между вершиной звёздчатой структуры и нуклеокапсидом может быть заполнено гидролитическими ферментами, которые нужны для проникновения вируса в клетку. Между капсидом и нуклеокапсидом были обнаружены внутренние белковые нити, которые предположительно обеспечивают стабильное положение второго внутри первого[20].
Неструктурные белки и РНК
[править | править код]Помимо структурных белков капсида, в составе вириона обнаруживают и другие белки, которые классифицируют на несколько функциональных групп:
- белки, участвующие в транскрипции,
- 5 субъединиц ДНК-зависимой РНК-полимеразы,
- 2 хеликазы (R350, L540),
- кэпирующий фермент,
- 4 фактора транскрипции (L377, L538, L544, R563),
- белки окислительных путей (предположительно помогают вирусу преодолеть окислительный стресс, связанный с активацией защитных систем клетки-хозяина) (9),
- белки, модифицирующие липиды и белки,
- 2 протеинкиназы,
- протеинфосфатаза,
- фосфоэстераза,
- липаза,
- белки, участвующие в метаболизме ДНК,
- топоизомеразы IA и IB,
- эндонуклеаза, корректирующая повреждения ДНК ультрафиолетовым светом[10].
Кроме белков и ДНК, из очищенных вирионов были выделены несколько различных мРНК, кодирующих ДНК-полимеразу (R322), главный белок капсида L425, TFII-подобный фактор транскрипции (R339), 3 аминоацил-тРНК-синтетазы (L124, L1164 и R663) и 4 неидентифицированных белка, специфичных для мимивируса. По-видимому, трансляция этих мРНК клеточным аппаратом биосинтеза белка необходима для начала репликации вируса. Другие ДНК-содержащие вирусы, такие как цитомегаловирус (Cytomegalovirus) и вирус простого герпеса (Herpes simplex virus type-1), также содержат мРНК[22].
Геном
[править | править код]Общая структура
[править | править код]Геном мимивируса, состоящий из линейной молекулы двухцепочечной ДНК, был полностью секвенирован в 2004 году[23][24]. Он содержит 1 181 404 пары оснований и является вторым крупнейшим известным геномом среди вирусов, уступая только Megavirus chilensis (по данным на 2012 год)[25]. Кроме того, мимивирус обладает бо́льшим объёмом генетической информации, чем как минимум 30 организмов, имеющих клеточное строение[26].
По сведениям на 2010 год в геноме мимивируса насчитывают 986 открытых рамок считывания, 6 из которых кодируют тРНК[23][27][28]. Такое количество белковых продуктов является очень большим для вируса — некоторые вирусы обходятся всего четырьмя минимально необходимыми белками[29]. Детальные исследования генома всё ещё продолжаются: исправляются ошибки секвенирования, обнаруживаются новые рамки считывания[30].
Несмотря на большой размер генома, он используется довольно эффективно: на долю кодирующей ДНК приходится около 90,5 % всего объёма генома, это близко к тому, что наблюдается у других крупных ядерно-цитоплазматических ДНК-содержащих вирусов. Открытые рамки считывания разделены между собой промежутками примерно в 157 пар нуклеотидов. Две цепочки ДНК, названные R (англ. right — правая) и L (англ. left — левая), кодируют примерно одинаковое количество генов (450 и 465 соответственно, по данным на 2010 год). В геноме мимивируса не обнаруживается признаков деградации, характерных для геномов паразитических бактерий, таких как псевдогены и мобильные генетические элементы. Содержание адениновых и тимидиновых нуклеотидов довольно высоко — 72 %, что ведёт к повышенному содержанию в белках аминокислот, кодируемых АТ-богатыми кодонами (например, изолейцина, аспарагина и тирозина). Вблизи концов молекулы ДНК были обнаружены инвертированные повторы длиной 617 пар нуклеотидов. Предполагают, что комплементарное взаимодействие этих участков может приводить к формированию Q-структуры — кольцевой ДНК с двумя небольшими хвостами[30].
Гены
[править | править код]Примерно для половины генов мимивируса не обнаружены гомологи в современных базах данных, и только для 24 % известна предполагаемая функция[28].
В геноме мимивируса были обнаружены гомологи практически всех ключевых генов, характерных для других крупных ядерно-цитоплазматических вирусов. В то же время данный геном содержит примерно вдвое больше генов, чем геномы родственных вирусов, причём среди этих генов много уникальных. Например, геном мимивируса кодирует несколько белковых компонентов аппарата трансляции: тирозил-, аргинил-, цистеил- и метионил-тРНК-синтетазы, гомологи факторов инициации трансляции eIF4E (L496), eIF4A (R458) и SUI1/eIF1 (R464), фактора элонгации трансляции eEF-1 (R624) и фактора терминации трансляции eRF1 (R726). Помимо генов белков, участвующих в трансляции, обнаружено 6 генов, которые предположительно кодируют тРНК, узнающие кодоны для лейцина, триптофана, гистидина и цистеина. Кроме того, мимивирус кодирует два гомолога РНК-урацил-5-метилтрансферазы (R405, R407) — фермента, метилирующего остаток урацила в тРНК и рРНК[30].
К другим необычным для вирусов генам относятся гены трёх типов топоизомераз и полного набора ферментов репарации, которые способны исправлять ошибки в ДНК, возникшие в результате действия окислителей, ультрафиолетового облучения и алкилирующих веществ. Также мимивирус кодирует ферменты углеводного, липидного и аминокислотного метаболизма[10][31].
Регуляция генома
[править | править код]Механизмы приспособления мимивируса к изменениям среды на протяжении многих поколений демонстрируют, наряду с признаками дарвинистической эволюции, признаки, соответствующие принципам ламаркизма. Так, например, у мимивируса в условиях пониженной конкуренции происходит репрессия некоторых генов. Это изменение наследуется следующими поколениями вируса, в некоторых случаях усиливаясь вплоть до полной инактивации этих генов. Предположительно, эффект является следствием худшей репарации менее используемых генов[32].
Другие особенности
[править | править код]Мимивирус является одним из немногих дцДНК-вирусов, в геноме которых обнаружена последовательность, кодирующая интеин. Интеин представляет собой белковый домен, который катализирует своё собственное вырезание из несущей молекулы и сшивание образовавшихся концов. Такая последовательность присутствует в гене ДНК-полимеразы B мимивируса[33].
Октамерная последовательность AAAATTGA была обнаружена примерно перед половиной генов мимивируса в положении от −80 до −50. Эта последовательность является TATA-подобным промоторным элементом и узнаётся транскрипционным аппаратом вируса на ранней стадии жизненного цикла[10]. Другая вырожденная АТ-богатая последовательность является поздним промотором[27].
Жизненный цикл
[править | править код]Клетки-хозяева
[править | править код]Первым известным хозяином мимивируса является амёба Acanthamoeba polyphaga. Попытки экспериментально инфицировать клетки других одно- и многоклеточных организмов показали, что только другие представители рода Acanthamoeba — A. castellanii и A. mauritaniensis — могут служить хозяевами данного вируса[22]. Некоторые данные указывают на то, что мимивирус может проникать в макрофаги человека и мышей и размножаться в них[7][1].
Цикл репликации
[править | править код]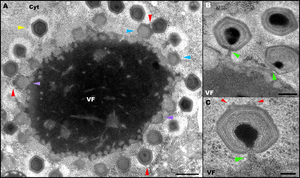
Мимивирус имеет 24-часовой литический (сопровождающийся лизисом клетки-хозяина) жизненный цикл с эклипс-фазой продолжительностью 4—5 часов[22]. Все стадии жизненного цикла протекают в цитоплазме клетки[35].
Заражение амёбы мимивирусом предположительно происходит по следующему сценарию:
- Вирионы мимивируса, напоминающие бактерий своими размерами и присутствием характерных полисахаридов на поверхности, поглощаются амёбой как пища в процессе эндоцитоза;
- Белковые нити частично лизируются в эндосомах, в результате чего капсид может взаимодействовать с эндосомальной мембраной;
- Капсид раскрывается в районе звёздчатой структуры, и его содержимое высвобождается в цитоплазму в результате слияния внутренней мембраны и мембраны эндосомы (это происходит примерно через 2 часа после инфицирования);
- После выхода коровой частицы (внутренней части нуклеокапсида) в цитоплазму, благодаря наличию в ней вирусного аппарата транскрипции, начинается синтез вирусных мРНК. Эти мРНК накапливаются внутри коровой частицы в виде гранул[35]. Предполагают, что первыми под действием вирусной РНК-полимеразы транскрибируются гены, которые находятся под контролем AAAATTGA-промотора (см. раздел Геном);
- Через 4—5 часов после заражения вирусная ДНК выходит из коровой частицы и деконденсируется, начинается её репликация. В результате рядом с пустой оболочкой коровой частицы формируется так называемая «вирусная фабрика» — место синтеза компонентов и сборки вирусных частиц[36]. Если в клетку проникли несколько вирусных частиц, то формируемые ими «фабрики» сливаются в одну по мере разрастания;
- Через 6—9 часов после заражения можно наблюдать процессы сборки капсидов и упаковки в них ДНК, которые происходят на периферии «вирусных фабрик». Необычным свойством мимивируса является то, что ДНК упаковывается и выходит из капсида через два разных отверстия[21];
- Через 14—24 часа после инфекции происходит лизис клетки амёбы и высвобождение вирионов, к этому моменту их накапливается в клетке более 300 единиц[30].
Патогенность
[править | править код]Существует гипотеза, что мимивирус может вызывать у людей некоторые формы пневмонии[7]. До сих пор были найдены лишь косвенные свидетельства в пользу этой гипотезы. Во-первых, было показано, что в условиях эксперимента мимивирус способен заражать человеческие макрофаги, проникая в клетки в процессе фагоцитоза, и реплицироваться в них[1]. Во-вторых, в нескольких исследованиях у небольшого количества пациентов, страдающих пневмонией, были обнаружены антитела против мимивируса[37][38]. Также был описан единичный случай развития пневмонии у лаборанта, который работал с культурами этого вируса. Содержание антител против мимивируса в его крови тоже было повышенным[39]. Тем не менее, присутствие антител против вируса само по себе не говорит о его патогенности, не исключено, что мимивирус просто обладает сильными иммуногенными свойствами[30].
С другой стороны, ни в одном из зарегистрированных случаев не удалось выделить вирус в чистом виде из образцов жидкостей, полученных от пациентов. Кроме того, исследования, в которых использовалась полимеразная цепная реакция, не обнаружили присутствия мимивируса у пациентов с пневмонией. В 2012 году группа Ванспоуна опубликовала результаты исследования больных пневмонией с целью определить роль мимивируса как возможного патогена. Ни у одного из 109 исследованных пациентов не был обнаружен мимивирус, и лишь у трёх были обнаружены антитела к нему[40]. В целом, вопрос о патогенности мимивируса для человека остаётся открытым, но в качестве охранной меры предлагается рассматривать его как организм II группы патогенности[30].
Вирофаги мимивируса
[править | править код]
Научная группа, открывшая мимивирус, также изолировала несколько других родственных ему вирусов, включая чуть более крупный мамавирус[англ.] (англ. Mamavirus). При изучении вирусных фабрик мамавируса было обнаружено, что на них также собираются небольшие вирионы другого вируса, который был назван Спутником (англ. Sputnik)[41]. Спутник, по всей видимости, сам не способен заражать клетки амёб и размножаться в них, но может делать это совместно с мама- или мимивирусом, что классифицирует его как вирус-сателлит. Спутник стал первым известным вирусом-сателлитом, содержащим двухцепочечную ДНК и размножающимся в эукариотических клетках. Однако авторы работы предлагают рассматривать этот вирус не просто как сателлит, а как вирофаг (вирус вируса) по аналогии с бактериофагами (вирусами бактерий)[42][43][28]. Разница в этих двух концепциях заключается в том, что вирусы-сателлиты полагаются на другой вирус и клетку-хозяина для своего размножения. Вирофаги же, как предполагается, воспроизводятся только за счёт репликативного аппарата вируса-хозяина, то есть являются паразитами исключительно другого вируса[30]. Хотя строгое доказательство ещё предстоит получить, некоторые факты говорят в пользу того, что Спутник действительно является вирофагом. Например, в его геноме присутствуют регуляторные элементы, характерные для мимивируса и узнаваемые его транскрипционным аппаратом (последовательности, близкие к позднему промотору мимивируса, сигналы полиаденилирования). Кроме того, присутствие Спутника снижает продуктивность размножения мимивируса: лизис клетки-хозяина происходит позже, образуются дефектные вирионы[41].
На сегодняшний день был открыт второй вирофаг мимивируса — штамм CL[44].
Эволюция и происхождение мимивируса
[править | править код]Эволюция
[править | править код]Мимивирус и другие крупные ядерно-цитоплазматические ДНК-содержащие вирусы обладают рядом свойств, которые не вписываются в традиционные представления о вирусах: крупный размер вирионов, присутствие в вирионе одновременно двух типов нуклеиновых кислот, большой размер и сложность генома, присутствие нехарактерных для вирусов генов (гены белков, участвующих в трансляции, репарации ДНК и фолдинге белков) и возможность выступать в качестве хозяина для другого вируса[15]. Эти факты возродили интерес к вопросу о происхождении и эволюции вирусов.
Было высказано две принципиально разных гипотезы о происхождении сложного генома мимивируса. Согласно первой из них, мимивирус и другие крупные ядерно-цитоплазматические ДНК-содержащие вирусы произошли от более сложного предка (клетки или вируса) путём редукционной эволюции и принадлежат к четвёртому домену живого[23]. По второй гипотезе, эволюция этих вирусов шла по пути усложнения и постепенного накопления генов, поступающих из геномов других организмов путём горизонтального переноса[45]. Фактически обе гипотезы опираются на данные сравнительной геномики и протеомики, которые могут быть интерпретированы по-разному, учитывая тот факт, что они отражают события, возможно, происходившие сотни миллионов лет назад. Относительно быстрые темпы эволюции вирусов и интенсивный горизонтальный перенос генов осложняет анализ и затрудняет построение филогенетических деревьев. Собственно факты, с которыми согласно большинство исследователей, заключаются в том, что более половины генов (и мотивов укладки белков) мимивируса не имеют известных гомологов. Другие данные и их интерпретация продолжают оставаться темой горячих споров.
В геноме мимивируса были обнаружены необычные для вирусов гены, ортологи которых присутствуют у организмов всех трёх доменов (гены аминоацил-тРНК-синтетаз, субъединиц РНК- и ДНК-полимераз). Анализ этих и других генов мимивируса, для которых известны гомологи, позволил определить его относительное положение на филогенетическом дереве. Однако, в зависимости от алгоритма анализа, были получены очень разные результаты. По мнению одних исследователей, линия, ведущая к современному мимивирусу, обособилась примерно в то же время, что и эукариотическая, или даже раньше[23][25]. Сходные результаты были получены и при сравнительном анализе типов белковых укладок[46]. Другие же учёные настаивают на том, что эти гены были приобретены мимивирусом в результате горизонтального переноса от представителей эу- и прокариот и что нет никаких оснований выделять вирусы в четвёртый домен живого[47][48]. Кроме того, большой размер генома мимивируса может быть объяснён особенностями занимаемой им экологической ниши, накладывающей меньшие ограничения на размеры генома. Существует мнение, что эти особенности позволили мимивирусу накопить большое количество копий гомологичных генов, которые возникали в результате дупликации генов и их дальнейшей независимой эволюции[16].
Происхождение
[править | править код]Вопрос о происхождении гигантских вирусов остаётся ещё более загадочным, чем вопрос их эволюции. Было высказано предположение, что представители группы крупных ядерно-цитоплазматических ДНК-содержащих вирусов (поксвирусы, иридовирусы, фикоднавирусы, мимивирусы и др.) ведут своё начало от более сложных (возможно клеточных) форм, таких как современные микоплазмы и риккетсии[49]. В пользу этой гипотезы говорит наличие в геноме крупных ДНК-содержащих вирусов большого количества «избыточных» генов, которые не являются строго необходимыми для размножения и функционально дублируют хозяйские. Сторонники этой точки зрения рассматривают, например, наличие у мимивируса и Megavirus chilensis неполного аппарата трансляции как признак того, что они произошли от свободноживущего или паразитического предка, у которого этот аппарат был полностью функционален[5][25]. По мере открытия новых гигантских вирусов учёные надеются получить больше информации о возможном общем предке крупных ядерно-цитоплазматических ДНК-содержащих вирусов.
Альтернативная гипотеза вирусного эукариогенеза, напротив, предполагает возникновение ядра эукариотических клеток из крупных ДНК-содержащих вирусов, подобных мимивирусам[49]. На разных этапах этого процесса новое примитивное ядро предположительно могло несколько раз возвращаться к существованию в форме гигантского вируса, что привело бы к формированию нескольких независимых групп вирусов.
Мимивирус и определение понятия «жизнь»
[править | править код]В 2000 году Международный комитет по таксономии вирусов официально объявил, что вирусы не относятся к живым организмам. Однако с открытием мимивируса эта идея была снова поставлена под сомнение[50][51]. Хотя мимивирус, как и любой другой вирус, не имеет генов рибосомальных белков и использует рибосомы хозяина, он формирует вирусные фабрики, которые функционируют относительно независимо от клетки. Было высказано мнение, что именно вирусные фабрики, а не метаболически неактивные вирусные частицы, и следует рассматривать как вирус[49]. Автор этой идеи полагает, что вирусная фабрика, осуществляющая репликацию ДНК, транскрипцию генов и синтез соответствующих белков с привлечением компонентов цитозоля, очень сильно напоминает клеточное ядро. С этой точки зрения, вирусные фабрики мимивируса кажутся гораздо ближе к живому, чем его вирион.
Тем не менее, многие учёные продолжают придерживаться более традиционного в последнее десятилетие мнения о том, что вирусы представляют собой неживые частицы[52]. Возможно, более точно на этот вопрос можно будет ответить с открытием новых гигантских вирусов.
См. также
[править | править код]- Mycoplasma genitalium — одна из самых маленьких известных бактерий.
- Candidatus Pelagibacter ubique — бактерия, обладающая одним из самых маленьких геномов.
- Наноархеоты — самые маленькие из известных одиночных клеток, самый маленький геном среди прокариот.
Примечания
[править | править код]- ↑ 1 2 3 Ghigo E., Kartenbeck J., Lien P., Pelkmans L., Capo C., Mege J. L., Raoult D. Ameobal pathogen mimivirus infects macrophages through phagocytosis // PLoS Pathog. — 2008. — Т. 4, вып. 6. — С. e1000087. — doi:10.1371/journal.ppat.1000087. — PMID 18551172. Архивировано 14 марта 2023 года.
- ↑ Таксономия вирусов (англ.) на сайте Международного комитета по таксономии вирусов (ICTV).
- ↑ ВИРУСЫ • Большая российская энциклопедия - электронная версия. bigenc.ru. Дата обращения: 15 марта 2020. Архивировано 5 февраля 2020 года.
- ↑ "World's biggest virus found in sea off Chile". London: Telegraph UK. 2011-10-11. Архивировано 15 января 2014. Дата обращения: 11 ноября 2011.
- ↑ 1 2 Arslan, D. et al. Distant mimivirus relative with a larger genome highlights the fundamental features of Megaviridae (англ.) // Proceedings of the National Academy of Sciences. — United States National Academy of Sciences, 2011. — Vol. 108. — P. 17486—17491. — doi:10.1073/pnas.1110889108.
- ↑ Xiao C., Chipman P. R., Battisti A. J., Bowman V. D., Renesto P., Raoult D., Rossmann M. G. Cryo-electron microscopy of the giant Mimivirus // J Mol Biol. — 2005. — Т. 353, вып. 3. — С. 493—496. — PMID 16185710.
- ↑ 1 2 3 Vincent A., La Scola B., Papazian L. Advances in Mimivirus pathogenicity // Intervirology. — 2010. — Т. 53, вып. 5. — С. 304—309. — doi:10.1159/000312915. — PMID 20551682.
- ↑ Xiao C., Rossmann M. G. Structures of giant icosahedral eukaryotic dsDNA viruses // Curr Opin Virol. — 2011. — Т. 1, вып. 2. — С. 101—109. — doi:10.1016/j.coviro.2011.06.005. — PMID 21909343. Архивировано 24 июня 2022 года.
- ↑ Яковенко Л. В. Мимивириды – новая ветвь на филогенетическом древе жизни // Биология : журнал. — 2008. — Т. 654. Архивировано 4 марта 2016 года.
- ↑ 1 2 3 4 5 6 Claverie J. M., Abergel C., Ogata H. Mimivirus // Curr Top Microbiol Immunol. — 2009. — Т. 328. — С. 89—121. — PMID 19216436. Архивировано 17 июня 2018 года.
- ↑ Highfield, Roger, «The Bradford bug that may be a new life form, Архивная копия от 3 января 2016 на Wayback Machine» Daily Telegraph, 15 October 2004.
- ↑ Wessner D. R. Discovery of the Giant Mimivirus // Nature Education. — 2010. — Т. 3, вып. 9. — С. 61. Архивировано 1 ноября 2020 года.
- ↑ Mimivirus (англ.). SIB Swiss Institute of Bioinformatics. Дата обращения: 3 февраля 2013. Архивировано 10 февраля 2013 года.
- ↑ 1 2 3 La Scola B., Audic S., Robert C., Jungang L., de Lamballerie X., Drancourt M., Birtles R., Claverie J. M., Raoult D. A giant virus in amoebae (англ.) // Science. — 2003. — Vol. 299, iss. 5615. — P. 2033. — PMID 12663918. Архивировано 23 июля 2013 года.
- ↑ 1 2 3 Colson P., de Lamballerie X., Fournous G., Raoult D. Reclassification of giant viruses composing a fourth domain of life in the new order Megavirales // Intervirology. — 2012. — Т. 55, вып. 5. — С. 321—332. — doi:10.1159/000336562. — PMID 22508375.
- ↑ 1 2 Koonin E. V. Virology: Gulliver among the Lilliputians // Curr Biol. — 2005. — Т. 15, вып. 5. — С. R167—169. — PMID 15753027. Архивировано 24 сентября 2015 года.
- ↑ Таксономия вирусов по состоянию на 2011 год на сайте ICTV. Дата обращения: 27 декабря 2012. Архивировано из оригинала 5 января 2013 года.
- ↑ Van Etten J. L. Giant Viruses (англ.) // American Scientist[англ.]. — Sigma Xi[англ.], 2011. — Vol. 99, iss. 4. — P. 304. — doi:10.1511/2011.91.304.
- ↑ 1 2 3 4 5 6 Xiao C., Kuznetsov Y. G., Sun S., Hafenstein S. L., Kostyuchenko V. A., Chipman P. R., Suzan-Monti M., Raoult D., McPherson A., Rossmann M. G. Structural studies of the giant mimivirus // PLoS Biol. — 2009. — Т. 7, вып. 4. — С. e92. — doi:10.1371/journal.pbio.1000092. — PMID 19402750. Архивировано 5 июля 2020 года.
- ↑ 1 2 3 4 Klose T., Kuznetsov Y. G., Xiao C., Sun S., McPherson A., Rossmann M. G. The three-dimensional structure of Mimivirus // Intervirology. — 2010. — Т. 53, вып. 5. — С. 268—273. — doi:10.1159/000312911. — PMID 20551678. Архивировано 5 июня 2022 года.
- ↑ 1 2 Zauberman N., Mutsafi Y., Halevy D. B., Shimoni E., Klein E., Xiao C., Sun S., Minsky A. Distinct DNA exit and packaging portals in the virus Acanthamoeba polyphaga mimivirus // PLoS Biol. — 2008. — Т. 6, вып. 5. — С. e114. — doi:10.1371/journal.pbio.0060114. — PMID 18479185. Архивировано 5 июня 2022 года.
- ↑ 1 2 3 4 Suzan-Monti M., La Scola B., Raoult D. Genomic and evolutionary aspects of Mimivirus // Virus Res. — 2006. — Т. 117, вып. 1. — С. 145—155. — PMID 16181700.
- ↑ 1 2 3 4 Raoult D, Audic S, Robert C., Abergel C., Renesto P., Ogata H., La Scola B., Suzan M., Claverie J. M. The 1.2-megabase genome sequence of Mimivirus (англ.) // Science. — 2004. — Vol. 306, iss. 5700. — P. 1344—1350. — PMID 15486256. Архивировано 24 сентября 2015 года.
- ↑ Полная последовательность генома Acanthamoeba polyphaga mimivirus в базе данных NCBI. Дата обращения: 28 декабря 2012. Архивировано 28 мая 2016 года.
- ↑ 1 2 3 Legendre M., Arslan D., Abergel C., Claverie J. M. Genomics of Megavirus and the elusive fourth domain of Life // Commun Integr Biol. — 2012. — Т. 5, вып. 1. — С. 102—106. — PMID 22482024. Архивировано 24 сентября 2019 года.
- ↑ Claverie J. M., Ogata H., Audic S., Abergel C., Suhre K., Fournier P. E. Mimivirus and the emerging concept of "giant" virus // Virus Res. — 2006. — Т. 117, вып. 1. — С. 133—144. — PMID 16469402.
- ↑ 1 2 Legendre M., Audic S., Poirot O., Hingamp P., Seltzer V., Byrne D., Lartigue A., Lescot M., Bernadac A., Poulain J., Abergel C., Claverie J. M. mRNA deep sequencing reveals 75 new genes and a complex transcriptional landscape in Mimivirus // Genome Res. — 2010. — Т. 20, вып. 5. — С. 664—674. — doi:10.1101/gr.102582.109. — PMID 20360389. Архивировано 14 сентября 2022 года.
- ↑ 1 2 3 Desnues C., Boyer M., Raoult D. Sputnik, a virophage infecting the viral domain of life // Adv Virus Res. — 2012. — Т. 82. — С. 63—89. — doi:10.1016/B978-0-12-394621-8.00013-3. — PMID 22420851.
- ↑ Prescott L. Microbiology. — Wm. C. Brown Publishers, 1993. — ISBN 0-697-01372-3.
- ↑ 1 2 3 4 5 6 7 Claverie J. M., Abergel C. Mimivirus and its virophage // Annu Rev Genet. — 2009. — Т. 43. — С. 49—66. — doi:10.1146/annurev-genet-102108-134255. — PMID 19653859.
- ↑ Piacente F., Marin M., Molinaro A., De Castro C., Seltzer V., Salis A., Damonte G., Bernardi C., Claverie J. M., Abergel C., Tonetti M. Giant DNA virus mimivirus encodes pathway for biosynthesis of unusual sugar 4-amino-4,6-dideoxy-D-glucose (Viosamine) // J Biol Chem. — 2012. — Т. 287, вып. 5. — С. 3009—3018. — doi:10.1074/jbc.M111.314559. — PMID 22157758.
- ↑ Colson P. and Raoult D. Lamarckian evolution of the giant Mimivirus in allopatric laboratory culture on amoebae // Front. Cell. Inf. Microbio.. — 2012. — Т. 91, вып. 2. — doi:10.3389/fcimb.2012.00091.
- ↑ Ogata H., Raoult D., Claverie J. M. A new example of viral intein in Mimivirus // Virol J. — 2005. — Т. 2. — С. 8. — PMID 15707490. Архивировано 1 мая 2023 года.
- ↑ Zauberman N., Mutsafi Y., Halevy D. B., Shimoni E., Klein E., Xiao C., Sun S., Minsky A. Distinct DNA exit and packaging portals in the virus Acanthamoeba polyphaga mimivirus // PLoS Biol. — 2008. — Т. 6, вып. 5. — С. e114. — doi:10.1371/journal.pbio.0060114. Архивировано 5 июня 2022 года.
- ↑ 1 2 Mutsafi Y., Zauberman N., Sabanay I., Minsky A. Vaccinia-like cytoplasmic replication of the giant Mimivirus // Proc Natl Acad Sci U S A. — 2010. — Т. 107, вып. 13. — С. 5978—5982. — doi:10.1073/pnas.0912737107. — PMID 20231474. Архивировано 2 августа 2022 года.
- ↑ Открыто уникальное поведение крупнейшего вируса. Membrana (12 апреля 2010). Дата обращения: 7 февраля 2013. Архивировано из оригинала 10 февраля 2013 года.
- ↑ La Scola B., Marrie T. J., Auffray J. P., Raoult D. Mimivirus in pneumonia patients // Emerg Infect Dis.. — 2005. — Т. 11, вып. 3. — С. 449—452. — PMID 15757563. Архивировано 30 апреля 2020 года.
- ↑ Berger P., Papazian L., Drancourt M., La Scola B., Auffray J. P., Raoult D. Ameba-associated microorganisms and diagnosis of nosocomial pneumonia // Emerg Infect Dis. — 2006. — Т. 12, вып. 2. — С. 248—255. — PMID 16494750. Архивировано 29 апреля 2023 года.
- ↑ Raoult D., Renesto P., Brouqui P. Laboratory infection of a technician by mimivirus // Ann Intern Med. 144(9):. — 2006. — Т. 144, вып. 9. — С. 702—703. — PMID 16670147. Архивировано 4 марта 2016 года.
- ↑ Vanspauwen M. J. et al. Infections with mimivirus in patients with chronic obstructive pulmonary disease // Respiratory Medicine. — 2012. — Т. 106, вып. 12. — С. 1690—1694. — doi:10.1016/j.rmed.2012.08.019. Архивировано 6 апреля 2017 года.
- ↑ 1 2 La Scola B., Desnues C., Pagnier I., Robert C., Barrassi L., Fournous G., Merchat M., Suzan-Monti M., Forterre P., Koonin E., Raoult D. The virophage as a unique parasite of the giant mimivirus (англ.) // Nature. — 2008. — Vol. 455, iss. 7209. — P. 100—104. — doi:10.1038/nature07218. — PMID 18690211.
- ↑ Helen Pearson. 'Virophage' suggests viruses are alive (2008). Дата обращения: 2 февраля 2013. Архивировано 10 февраля 2013 года.
- ↑ Александр Марков. Вирусы тоже болеют вирусными заболеваниями (8 сентября 2008). Дата обращения: 2 февраля 2013. Архивировано 10 февраля 2013 года.
- ↑ La Scola B., Campocasso A., N'Dong R., Fournous G., Barrassi L., Flaudrops C., Raoult D. Tentative characterization of new environmental giant viruses by MALDI-TOF mass spectrometry // Intervirology. — 2010. — Т. 53, вып. 5. — С. 344—353. — doi:10.1159/000312919. — PMID 20551686.
- ↑ Moreira D., López-García P. Comment on "The 1.2-Megabase Genome Sequence of Mimivirus" (англ.) // Science. — 2005. — Vol. 308, iss. 5725. — P. 1114. — doi:10.1126/science.1110820. — PMID 15905382.
- ↑ Nasir A., Kim K. M., Caetano-Anolles G. Giant viruses coexisted with the cellular ancestors and represent a distinct supergroup along with superkingdoms Archaea, Bacteria and Eukarya // BMC Evol Biol. — 2012. — Т. 12. — С. 156. — doi:10.1186/1471-2148-12-156. — PMID 22920653. Архивировано 4 октября 2013 года.
- ↑ Moreira D., Brochier-Armanet C. Giant viruses, giant chimeras: the multiple evolutionary histories of Mimivirus genes // BMC Evol Biol. — 2008. — Т. 8, № 12. — doi:10.1186/1471-2148-8-12. — PMID 18205905. Архивировано 24 сентября 2019 года.
- ↑ Williams T. A., Embley T. M., Heinz E. Informational gene phylogenies do not support a fourth domain of life for nucleocytoplasmic large DNA viruses (англ.) // PLOS One. — Public Library of Science, 2011. — Vol. 6, iss. 6. — P. e21080. — doi:10.1371/journal.pone.0021080. — PMID 21698163. Архивировано 17 октября 2022 года.
- ↑ 1 2 3 Claverie J. M. Viruses take center stage in cellular evolution // Genome Biol. — 2006. — Т. 7, вып. 6. — С. 110. — PMID 16787527. Архивировано 16 августа 2019 года.
- ↑ Mary C. [10.1126/science.335.6072.1035 Giant Viruses Revive Old Questions About Viral Origins] (англ.) // Science. — 2012. — Vol. 335, iss. 6072. — P. 1035. — PMID 22383822.
- ↑ Luketa S. New views on the megaclassification of life // Protistology. — 2012. — Т. 7, вып. 4. — С. 218—237.
- ↑ Moreira D., López-García P. Ten reasons to exclude viruses from the tree of life // Nat Rev Microbiol. — 2009. — Т. 7, вып. 4. — С. 306—311. — doi:10.1038/nrmicro2108. — PMID 19270719.
Литература
[править | править код]- Filée, Jonathan; Chandler, Michael. Unpacking the Baggage: Origin and Evolution of Giant Viruses // Viruses: Essential Agents of Life (неопр.). — Springer Netherlands, 2012. — С. 203—216. — ISBN 978-94-007-4899-6.
- Ghedin, Elodie, and Claverie, J. M., 2005, «Mimivirus relatives in the Sargasso sea», Virology Journal 2:62.
- Mutsafi Y., Fridmann-Sirkis Y., Milrot E., Hevroni L., Minsky A. Infection cycles of large DNA viruses: Emerging themes and underlying questions (англ.) // Virology : journal. — 2014.
- Raoult D., Audic S., Robert C., Abergel C., Renesto P., Ogata H., La Scola B., Suzan M., Claverie J. M. The 1.2-megabase genome sequence of Mimivirus. Science. 2004 Nov 19;306(5700):1344-50. PMID 15486256
- Yutin N., Wolf Y.I., Koonin EV. Origin of giant viruses from smaller DNA viruses not from a fourth domain of cellular life (англ.) // Virology : journal. — 2014.
Ссылки
[править | править код]- The Big Picture Book of Viruses — изображения мимивируса
- Учёные обнаружили паразитизм среди вирусов
- Мимивирус на сайте MicrobeWiki
- Press Release: Mimivirus: discovery of a giant virus, Paris, 28 March, 2003.
- GiantVirus.org
Эта статья входит в число избранных статей русскоязычного раздела Википедии. |