Карбонат стронция (TgjQkugm vmjkuenx)
| Карбонат стронция | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
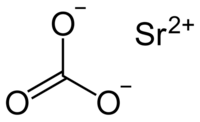
Карбонат стронция |
| Хим. формула | SrCO3 |
| Рац. формула | SrCO3 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 147,63 г/моль |
| Плотность | 3,785 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 1494 (под давлением) |
| • разложения | 1350 °C |
| Мол. теплоёмк. | 82,42 Дж/(моль·К) |
| Энтальпия | |
| • образования | -1227 кДж/моль |
| Классификация | |
| Рег. номер CAS | 1633-05-2 |
| PubChem | 15407 и 139148737 |
| Рег. номер EINECS | 216-643-7 |
| SMILES | |
| InChI | |
| RTECS | WK8305000 |
| ChemSpider | 14666 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Карбонат стронция, углекислый стронций — SrCO3, стронциевая соль угольной кислоты.
Нахождение в природе
[править | править код]В природе встречается в виде минерала стронцианита, имеющего наряду с целестином промышленное значение[1].
Физические и химические свойства
[править | править код]Бесцветные кристаллы, мало растворимые в воде (2⋅10−3г в 100 г H2O при 25 °C).
Имеются три модификации SrCO3: до 925 °C существует α-модификация с ромбической кристаллической решеткой типа арагонита (пространственная группа Pmcn), свыше 925 °C устойчива гексагональная β-модификация с кристаллической решеткой типа кальцита; наконец, при температуре более 1416 °C и давлении 2 МПа возникает γ-модификация кубической сингонии.
Реагирует с разбавленными соляной, азотной и уксусной кислотами с образованием соответствующих солей.
Под действием избытка углекислого газа и воды переходит в растворимый гидрокарбонат:
Разлагается при нагревании свыше 1350 °C:
Получение
[править | править код]- Прокаливание концентрата целестина с углем или коксом с последующим переводом полученного сульфида стронция с помощью диоксида углерода в карбонат стронция[2].
- Обработка хлорида стронция карбонатом аммония или взаимодействием углекислого газа с оксидом, гидроксидом или другими водорастворимыми солями стронция[3].
Применение
[править | править код]Карбонат стронция является сырьем для производства многих химических соединений стронция различного назначения Структура потребления соединений стронция по конечным областям использования[2]
- для красного цвета 4 %
- стекло (цветные телевизоры, компьютеры, радары, различные дисплеи) — 68 %;
- светящиеся пигменты и краски (фосфора)- изготовление — 2 %
- пиротехника, сигналы — 14 %;
- ферритные керамические магниты — 9 %;
- пигменты — 2 %;
- электролитическое производство цинка — 2 %;
- другие — 3 %.
Стекольная промышленность
[править | править код]Карбонат стронция при добавлении в стекло делает последнее стойким к радиации и действию рентгеновских лучей. Это свойство используют для выпуска электронно-лучевых трубок.
Электротехника
[править | править код]Карбонат стронция применяют для производства высококачественных ферритов — керамических магнитов, необходимых в электротехнике для производства портативных электромоторов.
Примечания
[править | править код]- ↑ СТРОНЦИЙ — статья из энциклопедии «Кругосвет»
- ↑ 1 2 Архивированная копия. Дата обращения: 9 июня 2009. Архивировано 25 февраля 2007 года.
- ↑ Важнейшие соединения стронция. Дата обращения: 9 июня 2009. Архивировано из оригинала 2 апреля 2009 года.


