Хлорид молибдена(III) (}lkjn; bklnQ;yug(III))
Перейти к навигации
Перейти к поиску
| Хлорид молибдена(III) | |
|---|---|
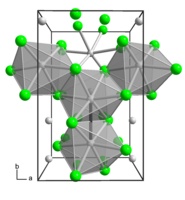 | |
| Общие | |
| Систематическое наименование |
Хлорид молибдена(III) |
| Традиционные названия | Хлористый молибден |
| Хим. формула | MoCl3 |
| Физические свойства | |
| Состояние | тёмно-красные кристаллы |
| Молярная масса | 202,30 г/моль |
| Плотность | 3,578 г/см³ |
| Классификация | |
| Рег. номер CAS | 13478-18-7 |
| PubChem | 83515 и 9815611 |
| Рег. номер EINECS | 236-775-9 |
| SMILES | |
| InChI | |
| ChEBI | 30626 |
| ChemSpider | 75350 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Хлорид молибдена(III) — неорганическое соединение, соль металла молибдена и соляной кислоты с формулой MoCl3, тёмно-красные кристаллы, плохо растворимые в воде, образует кристаллогидрат.
Получение
[править | править код]- Восстановление хлорида молибдена(V) водородом:
- Восстановление хлорида молибдена(V) порошкообразным молибденом:
- Разложение (диспропорционирование) при нагревании хлорида молибдена(IV):
- Действие хлористого водорода на нагретый бромид молибдена(III):
Физические свойства
[править | править код]Хлорид молибдена(III) образует тёмно-красные кристаллы, не растворяется в воде, этаноле, диэтиловом эфире.
Образует кристаллогидрат состава MoCl3•3H2O.
Химические свойства
[править | править код]- Разлагается при сильном нагревании в инертной атмосфере:
- Медленно реагирует с кислородом воздуха:
- Реагирует с водными растворами щелочей:
Литература
[править | править код]- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1992. — Т. 3. — 639 с. — ISBN 5-82270-039-8.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.
Это заготовка статьи о неорганическом веществе. Помогите Википедии, дополнив её. |






