Рак шейки матки (Jgt oywtn bgmtn)
| Рак шейки матки | |
|---|---|
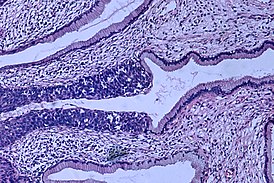 Гистологическая картина аденокарциномы на ранней стадии | |
| МКБ-11 | 2C77 |
| МКБ-10 | C53 |
| МКБ-10-КМ | C53.9 и C53 |
| МКБ-9 | 180 |
| МКБ-9-КМ | 180.9[1] и 180[1] |
| OMIM | 603956 |
| DiseasesDB | 2278 |
| MedlinePlus | 000893 |
| eMedicine | med/324 radio/140 |
| MeSH | D002583 |
Рак ше́йки ма́тки — злокачественное новообразование в области шейки матки. Гистологически различают две его основные разновидности: аденокарцинома и плоскоклеточный рак. В настоящее время считается доказанной связь заболеваемости вирусом папилломы человека и риском развития рака шейки матки.[2]
Значимость и распространённость
[править | править код]Исследования вопроса заболеваемости раком шейки матки проводились ещё в XIX веке, и полученные результаты показывали связь активности половой жизни и частоты встречаемости рака. Современные исследования подтверждают эти данные, наблюдается связь между частотой смены половых партнёров и риском заболевания раком шейки матки.[3] В России в 2002 году было зарегистрировано 12 285 случаев заболевания раком шейки матки.[4] Данное заболевание наиболее часто встречается у женщин среднего возраста (35—55 лет), в 20 % случаев обнаруживается в возрасте старше 65 лет, в молодом возрасте встречается относительно редко. Заболеваемость раком шейки матки значительно превышает заболеваемость другими опухолями женской половой системы.[4] В начале XXI века отмечается увеличение больных раком шейки матки на поздних стадиях: доля рака IV стадии, по разным данным, составляет 37,1 % — 47,3 %.[2][5]
Классификация
[править | править код]При классификации рака шейки матки используется стандартная TNM-классификация злокачественных новообразований.[6]
- Тх — недостаточно данных для оценки опухоли.
- Т0 — первичная опухоль не определяется.
- Tis — карцинома преинвазивная. Стадия по FIGO 0
- Т1 — Рак, ограниченный шейкой матки (без учёта тела матки). Стадия по FIGO 1
- Т1а — Инвазивная опухоль, обнаруживается только микроскопически. Стадия по FIGO 1а
- Т1а1 — Инвазия в строму до 3,0 мм в глубину и до 5,0 мм поверхности. Стадия по FIGO 1а 1
- Т1а2 — Инвазия в строму до 5,0 мм в глубину и до 7,0 мм по поверхности. Стадия по FIGO 1а 2
- T1b — Клинически определяемый очаг поражения, ограниченный шейкой матки или микроскопически определяемое поражение большего размера, чем Т1А/1A2. Стадия по FIGO 1b
- T1b1 — Клинически определяемый очаг поражения более 5,0 мм до 4,0 см в наибольшем измерении. Стадия по FIGO 1b1
- T1b2 — Клинически определяемый очаг поражения более 4,0 см. Стадия по FIGO 1b1
- Т2 — Опухоль шейки матки с распространением за пределы матки, но без прорастания стенки таза или нижней трети влагалища. Стадия по FIGO 2
- T2a — Без инвазии в параметрий. Стадия по FIGO 2a
- T2b — С инвазией в параметрий. Стадия по FIGO 2b.
- Т3 — Рак шейки матки с распространением на стенку таза, поражение нижней трети влагалища, нарушение функции почки. Стадия по FIGO 3.
- Т3а — Опухоль поражает нижнюю треть влагалища, но не распространяется на стенку таза, и не повреждает почки. Стадия по FIGO 3a.
- T3b — Опухоль распространяется на стенку таза и/или приводит к гидронефрозу и нефункционирующей почке. Стадия по FIGO 3b.
- Т4 — Опухоль распространяется на слизистую оболочку мочевого пузыря или прямой кишки и/или выходит за пределы малого таза. Стадия по FIGO 4а.
- M1 — Отдалённые метастазы. Стадия по FIGO 4b.
FIGO – the International Federation of Gynecology and Obstetrics.
Этиология
[править | править код]В настоящее время выявлены факторы, которые повышают риск заболевания раком шейки матки. К ним относятся[2][7]:
- Раннее начало половой жизни (до 16 лет).
- Частая смена сексуальных партнёров (более 2—3 в год).
- Курение.
- Инфицирование вирусом папилломы человека.
В большинстве случаев фактором риска развития рака является вирус папилломы человека 16-го и 18-го серотипов. Вирусы данных серотипов ответственны за 65—75 % случаев возникновения рака шейки матки. Заражение вирусом папилломы человека происходит преимущественно половым путём, а барьерные средства контрацепции зачастую обладают недостаточной эффективностью в защите от инфицирования ВПЧ.[7]
Несмотря на то, что инфицирование при половом контакте с носителем ВПЧ достигает 75 %, в 90 % случаев вирус достаточно быстро уничтожается иммунной системой, и только если вирусу удаётся преодолеть иммунную защиту, развивается персистирующее течение заболевания, сопровождающееся изменениями в эпителии шейки матки.[7]
Исследования ВОЗ показали, что женщина, имевшая в течение жизни более 10 половых партнёров, имеет в 3 раза больший риск заболеть раком шейки матки. Также у женщин, страдающих ВПЧ, их постоянные половые партнёры в 5 раз чаще, чем мужчины в прочей популяции, имели более 20 половых партнёров.[7]
Патогенез
[править | править код]Злокачественные новообразования возникают в результате повреждения механизмов апоптоза. В случае рака шейки матки антионкогенную активность проявляют гены p53 Rb. При персистирующей инфекции вирусом папилломы человека эти антионкогены блокируются белками, производимыми вирусными генами Е5 и Е6. Белок, синтезируемый геном Е6, инактивирует опухолевый супрессор, запускающий механизм клеточной смерти бесконтрольно пролиферирующих клеток. Кроме того, данный белок активирует теломеразу, что увеличивает шансы возникновения бессмертных клонов клеток и, как следствие, развития злокачественных образований. Белок, синтезируемый геном Е6, не активен в отсутствие белка, синтезируемого геном Е7. Белок, вырабатываемый геном Е7, способен и самостоятельно вызывать опухолевую трансформацию клеток, но его действие значительно усиливается в присутствии белка, синтезируемого Е6. Блок Е7 блокирует циклин-зависимые киназы р21 и р26, что позволяет повреждённой клетке начать делиться. Таким образом мы видим, что вирус папилломы человека в результате своей жизнедеятельности повреждает противоопухолевую защиту клетки, значительно увеличивая риск развития злокачественных новообразований.[7][8]
Клиническая картина
[править | править код]Симптоматика на ранних стадиях может отсутствовать или проявляться в виде трудно дифференцируемого дискомфорта. На более поздних стадиях развития заболевания могут возникать следующие клинические признаки.[9]
- Патологические вагинальные кровотечения.
- Кровотечения после полового акта, спринцевания или вагинального осмотра гинекологом.
- Изменения характера и длительности менструации.
- Возникновение кровянистого отделяемого во влагалище после наступления менопаузы.
- Боль в области малого таза.
- Боль во время полового акта.
Все приведённые выше клинические признаки неспецифичны. Также развитие рака шейки матки может сопровождаться системными эффектами, например:
- Нарастающая слабость, утомляемость.
- Быстрая потеря веса.
- Длительно сохраняющаяся субфебрильная температура, не превышающая 37,5° С.
- Анемия и повышение СОЭ.
Отсутствие характерных клинических признаков и отсутствие жалоб в дебюте заболевания значительно затрудняют раннюю диагностику и при отсутствии регулярного гинекологического осмотра приводят к поздней диагностике заболевания, значительно ухудшающей прогноз выздоровления.
Диагностика
[править | править код]Этот раздел не завершён. |
В связи со стёртостью клинических проявлений и отсутствием специфической клиники наиболее эффективным методом диагностики являются регулярные гинекологические осмотры, призванные выявить ранние стадии злокачественных новообразований.[2]
Скрининговым методом, позволяющим выявить рак шейки матки на разных стадиях развития, является цитологическое исследование. Данные сравнительного анализа показывают, что оптимальным по эффективности и трудозатратам является обследование раз в 2—3 года. Ежегодные обследования увеличивают трудозатраты в 3 раза, а частота обнаружения новообразований возрастает только на 2 %. Достаточно часто в поздней диагностике виноваты сами больные, когда они, при обнаружении у себя бессимптомно текущего рака шейки матки, своевременно не начинают лечение и обращаются за медицинской помощью на поздних стадиях, когда эффективность терапии во много раз ниже, чем на ранних этапах.[2]
Основным методом диагностики является кольпоскопия, которая по мере необходимости расширяется различными дополнительными манипуляциями. Так, в случае скрининга проводится цитологическое исследование мазков отпечатков. Также шейка матки может обрабатываться уксусной кислотой для выявления плоских кондилом, которые будут проявляется как пятна другого цвета, на поверхности нормальной шейки. В случае подозрения на наличие атипичных клеток проводится кольпоскопия с биопсией. Признаком предраковых состояний является обнаруживаемый при цитологическом обследовании пойкилоцитоз. Предраковые состояния не всегда приводят к развитию злокачественных новообразований, но их наличие является плохим прогностическим признаком в отношении риска возникновения рака шейки матки.[2]
К диагностике рака шейки матки относятся такие исследования как:
- УЗИ
- МРТ с контрастом
- КТ или ПЭТ КТ с контрастом
- Ректо-вагинальное исследование
- Кольпоскопия
- Мазок на цитологию.
- Взятие крови на маркер SCC (при плоскоклеточной карциноме).
Так же перед началом лечения нужно выполнить по назначению врача такие исследования как:
- УЗИ органов малого таза
- УЗИ вен нижних конечностей
- ФКС (гастроскопия)
- Колоноскопия
- Анализ крови на ВИЧ, сифилис, гепатит
- Общий анализ крови
- Общий анализ мочи
- Биохимический анализ крови
- Биопсия.
- Раздельно-диагностическое выскабливание.
Лечение
[править | править код]Этот раздел не завершён. |
Лечение рака шейки матки комплексное, оно может сочетать в себе хирургическое лечение, лучевую терапию и химиотерапию.[10] Ранее считалось, что наиболее эффективным при лечении рака шейки матки является сочетание хирургического и лучевого методов лечения. Ряд исследований, проведённых в 1999—2000 годах, показал, что добавление химиотерапии значительно повышает эффективность лучевой терапии.[11] В период с 2005—2020 год сложилась тактика лечения рака шейки матки основанная на применении неоадъювантной химиотерапии перед проведением радикальной операции.
Так же стоит отменить, что в Западной Европе практика лечения больных раком шейки матки основана на применении операции+неоадъювантная или адъювантная химиотерапия, тогда как в США за основу принято химиолучевое лечение, которое там применяется начиная с первой стадии заболевания.
Комбинированное лечение показано во всех случаях наличия регионарного метастазирования.
Ряд крупных авторов полагает, что будущее в терапии рака шейки матки за персонализированным подходом в лечении каждой больной. С 2016 года проводят клинические исследования по использованию таргетных препаратов и иммунотерапии, в частности с привязкой результатом иммуногистологического исследования операционного материала. В России персонализированный подход в лечении больных раком шейки матки применяют все чаще.
Хирургическое лечение
[править | править код]При распространённых инвазивных формах рака шейки матки применяется расширенная гистерэктомия по методу Вертгейма—Мейгса, суть которой заключается в одномоментном иссечении тазовой клетчатки с заключёнными в ней лимфоузлами, удалении матки с придатками и не менее трети влагалищной трубки. В некоторых случаях производится экзентерация таза, но в настоящее время данный метод применяется относительно редко в связи с его высокой травматичностью для больной и эффективностью, незначительно превышающей гистерэктомию.[10]
Так же в ряде стран применяется такая операция как тотальная мезометрэктомия — когда производят терапевтическое удаление регионарных лимфатических узлов и в обязательном порядке полностью иссекают мезометрий — широкую связку матки, проходящую над прямой кишкой (немецкий профессор M. Hockel добился при мезометректомии хороших показателей выживаемости).
Лучевая терапия
[править | править код]Лучевая терапия является ведущим методом лечения рака шейки матки и зачастую, в сочетании с химиотерапией, единственно возможным на 3—4 стадии в связи с невозможностью хирургического вмешательства. Применяется дистанционная гамма-терапия. Разовая доза, подаваемая на область воздействия, составляет 2 грей. Как правило, дистанционная гамма терапия сочетается со внутриполостным облучением шейки матки.[10]
Химиотерапия
[править | править код]В сочетании с лучевой терапией проводится полихимиотерапия несколькими цитостатическими препаратами. С одной стороны, эта терапия позволяет повысить эффективность лучевой терапии, добиться снижения дозы облучения и снизить шансы возникновения радиоиндуцированных опухолей. С другой стороны, сочетание химио- и лучевой терапии плохо переносится больными и приводит к усилению побочных эффектов. Ряд специалистов придерживаются мнения, что курсовая полихимиотерапия в сочетании с лучевой терапией малоэффективна и даже опасна.
Однако многие специалисты сходятся во мнении, что регионарная внутриартериальная химиотерапия цитостатиками желательна при проведении лучевой терапии, исследования показали повышение выживаемости больных, получавших подобное сочетание.[10]
Считается доказанной эффективность введения на фоне проведения лучевой терапии препаратов платины (цисплатин).[10] Некоторые авторы считают эффективней схему цисплатин/карбоплатин + радикальная лучевая терапия (дистанционное облучение + брахитерапия) в лечении местно-распространённых форм рака шейки матки.
В последние года наметилось перспективное направление в лечении рака шейки матки с применением неоадъювантной и адъювантной химиотерапии.
Неоадьювантная химиотерапия проводится при местно-распространенных стадиях (IB, IIA, IIB в некоторых случаях IIIB) с целью уменьшить размер опухоли и возможные очаги метастазирования (в параметриях и лимфатических узлах), что позволяет провести радикальную операцию с соблюдением правил абластики. В ряде онкологических центрах и отделений клиник во время операции проводят срочное гистологическое исследование лимфоузлов, на основании которого проводится тазовая и параортальная лимфодиссекция с резекцией параметриев. Не редко во время операции проводят внутреннюю обработку операционной зоны цитостатиками. Это случается когда клинические (ректально-вагинальный осмотр) и лучевые методы диагностики не отразили степень распространённости процесса и нужно нивелировать определившиеся во время операции факторы неблагоприятного прогноза. При этом нередко после операции назначают курсы адъювантной химиотерапии или химиолучевой терапии.
Адьювантная химиотерапия проводится после операции, когда выявлены риски прогрессирования заболевания при гистологическом исследовании операционного материала (лимфоваскулярная инвазия, положительный край резекции, наличие метастазов в регионарных лимфатических узлах) и после лучевой терапии (с целью повышения эффективности ЛТ и как дополнение к химиолучевой терапии в зависимости от группы риска больной).
Иммунотерапия
[править | править код]В настоящее время активно изучается вопрос сохранения иммунитета при лучевой и химиотерапии с целью обеспечения возможности организму задействовать и свои противоопухолевые механизмы. Считается, что относительно эффективным является введение интерферонов; относительно дозировки препаратов в научной среде идут активные дискуссии, и единого консенсусного мнения в настоящее время не существует.[10]
С 2015 по 2020 год проходят многофазные клинические исследования по иммунотерапии рака шейки матки, которые дают надежду на появление новых эффективных методов лечения больных.
Таргетная терапия
[править | править код]- Моноклональные антитела: пембролизумаб, кадонилимаб[англ.][12].
- Коньюгаты антитело-препарат: тизотумаб ведотин
Профилактика
[править | править код]Этот раздел не завершён. |
Для женщин, начиная с 30-летнего возраста, рекомендован скрининг для выявления предракового состояния и активного онкопроцесса рака шейки матки. Регулярный скрининг позволяет выявить развитие предраковых изменений в эпителии шейки матки и своевременно провести предупредительную терапию (для удаления перерождающихся клеток используется криокоагуляция, электрокоагуляцию или другой метод)[13].
Также для предотвращения рака шейки матки используется вакцинация против ВПЧ. На 2020 год существует три вакцины, одна — только против ВПЧ16 и ВПЧ18, которые вызывают 70 % случаев рака шейки матки, вторая эффективна также против ВПЧ6 и ВПЧ11, которые вызывают кондиломы, третья направлена против семи видов онкогенных ВПЧ (кроме 16 и 18, известны ещё пять видов ВПЧ, которые вызывают около 20 % известных случаев рака шейки матки) и двух кондиломогенных ВПЧ. Наиболее эффективна вакцинация девочек между 9 и 14 годами, до начала половой жизни — такая вакцинация предотвращает заболевание ВПЧ и индуцированным им раком шейки матки[14].
Вакцинация против ВПЧ не означает, что скрининг становится не нужен. Вакцинная защита дополняет скрининг, который при этом помогает выявить случаи, от которых вакцинация не смогла защитить[14].

Важную роль в профилактике рака шейки матки играет профилактика заражения вирусом папилломы человека. В настоящее время в России рекомендована вакцинопрофилактика папилломавирусной инфекции девочкам 13—15 лет. В некоторых странах прививают и мальчиков препубертатного возраста, с целью сократить циркуляцию вируса папилломы. Вакцинация проводится вакцинами Гардасил с интервалом 0-2-6 или Церварикс с интервалом 0-1-6. Некоторые авторы оспаривают роль вакцинации для предупреждения развития рака шейки матки. В основном все сходятся, что важно регулярно проводить скрининг рака шейки матки (PAP-тест, кольпоскопия и пр.), вести здоровый образ жизни (отказ от курения и алкоголя, подвижный образ жизни и пр.).[источник не указан 1349 дней]
Проблема заболеваемости раком шейки матки в России актуальна как никогда. Заболевание молодеет, всё чаще его выявляют у женщин 25-35 лет. Так же отмечается существенный рост заболеваемости. [источник не указан 1349 дней]
Профессор В. М. Мирабишвили в 1987 году заявил на съезде онкологов СССР, что к 1995 году в стране заболеваемость раком шейки матки сойдёт на нет. После этого съезда в стране произошёл ряд изменений, появились проблемы со скринингом и регулярной диспансеризацией населения. Это привело к тому, что заболеваемость раком шейки матки и его терапия в России оказалась на уровне развивающихся стран, в которых это заболевание выявляют часто в прогностически неблагоприятных стадиях. В 2013 году заболеваемость раком шейки матки в России вернулась к уровню 1970 года. Для сравнения, в Австралии вакцинация и скрининг населения привели практически к искоренению этого заболевания[15].
Стоит отметить, что рак шейки матки легкодоступен для диагностике уже на уровне местных районных консультаций. Главное в предупреждении развития рака шейки матки это онкологическая настороженность гинеколога и пациента. Женщина должна знать о необходимости регулярного посещения гинеколога для взятия мазка на цитологию, поскольку в зеркалах рак шейки матки становится заметен уже на продвинутых стадиях (когда на глаз видна васкуляризация эпителия, шейка становится бочкообразной, видны экзофитные образования), когда часто становятся недоступны органосохраняющие операции. Женщина не должна пропускать такие тревожные симптомы как контактные кровотечения (к примеру после полового акта), выделение крови из влагалища при натуживании при дефекации, появление ранее не характерных выделений (слизистых, сукровичных) — часто это стойкие водяные жёлтые выделения. Особенно если это сопровождается нерегулярным циклом, усталостью, частой сменой настроения.[источник не указан 1349 дней]
Прогноз
[править | править код]Прогноз условно благоприятен и зависит от стадии, на которой было выявлено заболевание. В России относительная пятилетняя выживаемость на ранних стадиях составляет около 92 %. Общая выживаемость, включающая и поздние стадии заболевания, составляет 72 %.[4] По данным других источников, 5-летняя выживаемость при первой стадии составляет 78,1 %, при второй — 57 %, при третьей — 31 %, при четвёртой — 7,8 %.[5] При этом эффективность лечения зависит от настроя самого пациента, его отказ от вредных привычек, проведение грамотной диагностики, профессионализма хирурга/радиотерапевта/химиотерапевта и обеспечение медицинского учреждения необходимым оборудованием.
Примечания
[править | править код]- ↑ 1 2 Disease Ontology (англ.) — 2016.
- ↑ 1 2 3 4 5 6 (PDF) Новик, В. И. Эпидемиология рака шейки матки. Факторы риска скрининг. «Практическая онкология». Т. 3, № 2 (2002). Дата обращения: 8 июня 2009. Архивировано 1 марта 2004 года.
- ↑ Предрак и рак шейки матки. ЦИР. Дата обращения: 8 июня 2009. Архивировано 1 апреля 2012 года.
- ↑ 1 2 3 www.medmax.ru Рак шейки матки, симптомы, лечение. Дата обращения: 8 июня 2009. Архивировано из оригинала 11 июня 2009 года.
- ↑ 1 2 Черкасский областной онкологический диспансер. Этиология и патогенез рака шейки матки. Дата обращения: 8 июня 2009. Архивировано из оригинала 4 июля 2009 года.
- ↑ Рак шейки матки. Классификация. Дата обращения: 8 июня 2009. Архивировано 1 сентября 2009 года.
- ↑ 1 2 3 4 5 (PDF) Гурцевич, В. Э. Рак шейки матки: Причины, следствия, профилактика. Журнал «СПИД, рак и общественное здоровье». Т. 11, № 1 (2007). Дата обращения: 8 июня 2009. Архивировано из оригинала 24 февраля 2015 года.
- ↑ Хансон, К. П. Современные представление о канцерогенезе рака шейки матки. Журнал «Практическая онкология» том 3 № 3 (2002). Дата обращения: 9 июня 2009. Архивировано 8 ноября 2005 года.
- ↑ Симптомы рака шейки матки. Дата обращения: 8 июня 2009. Архивировано 2 мая 2009 года.
- ↑ 1 2 3 4 5 6 (PDF) Максимов, С. Я. Комбинированное лечение рака шейки матки. «Практическая онкология». Т. 3, № 3 (2002). Дата обращения: 8 июня 2009. Архивировано 8 ноября 2005 года.
- ↑ ASCO 2001: рак яичников и шейки матки. Тюляндин С. А. Российский онкологический научный центр им. Н. Н. Блохина РАМН, Москва. Дата обращения: 9 июня 2009. Архивировано 2 января 2005 года.
- ↑ Cadonilimab: First Approval (англ.) // Drugs. : journal. — 2022. — doi:10.1007/s40265-022-01761-9. — PMID 35986837.
- ↑ ВОЗ, 2020, Screening and treatment of pre-cancer lesions.
- ↑ 1 2 ВОЗ, 2020, HPV vaccination.
- ↑ Максимов С. Я. Комбинированное лечение рака шейки матки : видео. // II конференция «Инновации в онкогинекологии» совместно с ESGO. Секция хирургия рака шейки матки. / Петербургский онкологический форум «Белые ночи». — 2015. — НМИЦ онкологии им. Н. Н. Петрова
Литература
[править | править код]- Шайн А. А. Онкология. Учебник для студентов медицинских вузов. — Медицинское информационное агентство, 2004. — 544 с.
- Ганцев Ш. X. Онкология. Учебник для студентов медицинских вузов. — 2-е издание, исправленное и дополненное. — Москва: Медицинское информационное агентство, 2006. — 488 с. — ISBN 5-89481-418-9.
- Вернер П., Зедерль Ю. Радикальная операция Вертгейма при раке шейки матки = Die wertheimsche Radikaloperation bei carcinoma colli uteri. Von P. Werner und J. Sederl. Wien-Innsbruck, Schwarzenberg, 1952 / Пауль Вернер, Юлиус Зедерль; Пер. с нем. Н. И. Короткина; Под ред. и с предисл. проф. Л. С. Персианинова. — М.: Медгиз, 1960. — 75 с.
Ссылки
[править | править код]- Human papillomavirus (HPV) and cervical cancer : [арх. 14 апреля 2021]. — ВОЗ, 2020. — 11 ноября.
- Палийчук О. В., Полищук Л. З. Роль инфекционных факторов в этиологии и патогенезе интраэпителиальной неоплазии и рака шейки матки. Дата обращения: 8 июня 2009. Архивировано из оригинала 1 апреля 2012 года.
- Рак шейки матки : Список статей : [арх. 01.04.2012]. — Российский онкологический сервер. — Дата обращения: 09.06.2009.
- Рак шейки матки, Европейская школа онкологии, видеолекция.
- Современные подходы к хирургическому лечению шейки матки Доклад кмн Морхова К. Ю. на онкологическом съезде «Белые ночи». 2015/
- Рак шейки матки. Доклад кмн Морхова К. Ю. на конференции RUSSKO 2014.
- Рак шейки матки: хирургическое лечение или лучевая терапия. Профессор В. М. Нечушкина: Конференция «Онкогинекология — рак шейки матки», 23-24 марта 2018 г., Москва
- Неоадъювантная химиотерапия и радикальные операции при раке шейки матки стадий IB2 — IIIB. Диссертация Оводенко Д. Л. 2020
- Адьювантная химиотерапия при раке шейки матки. Хохлова С. В.: Конференция «Онкогинекология — рак шейки матки», 23-24 марта 2018 г., Москва
- Хирургия инвазивного рака шейки матки. Оводенко Дмитрий Леонидович, Хабас Григорий Николаевич, Макарова Анна Семёновна, Серёгин Александр Александрович, Голицына Юлия Сергеевна, Ашрафян Лев Андреевич, Москва 2019