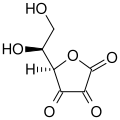
Дегидроаскорбиновая кислота (:yin;jkgvtkjQnukfgx tnvlkmg)
| Дегидроаскорбиновая кислота | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
(5"R")-5-[(1"S")-1,2-дигидроксиэтил]оксолан-2,3,4-трион |
| Хим. формула | C6H6O6 |
| Физические свойства | |
| Молярная масса | 174,108 г/моль |
| Классификация | |
| Рег. номер CAS | 490-83-5 |
| PubChem | 440667 |
| Рег. номер EINECS | 207-720-6 |
| SMILES | |
| InChI | |
| ChEBI | 27956 |
| ChemSpider | 389547 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Дегидроаскорбиновая кислота (ДГК) представляет собой окисленную форму аскорбиновой кислоты (витамина С). Он активно импортируется в эндоплазматический ретикулум клеток через переносчики глюкозы[1]. Он задерживается там путем восстановления обратно до аскорбата глутатионом и другими тиолами[2]. Свободный химический радикал семидегидроаскорбиновой кислоты (SDA) также принадлежит к группе окисленных аскорбиновых кислот.
Структура и физиология
[править | править код]Внизу: дегидроаскорбиновая кислота (номинальная окисленная форма витамина С).
Хотя существует натрий-зависимый переносчик витамина С, он присутствует в основном в специализированных клетках, в то время как переносчики глюкозы, наиболее заметным из которых является GLUT1, транспортируют витамин С (в его окисленной форме, ДГК)[3] в большинстве клеток, где происходит рециркуляция. обратно к аскорбату генерирует необходимый кофактор фермента и внутриклеточный антиоксидант (см. Транспорт в митохондрии).
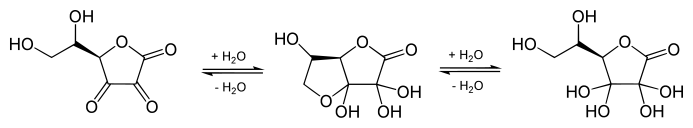
Структура, показанная здесь для DHA, является обычно показанной структурой учебника. Однако этот 1,2,3-трикарбонил слишком электрофилен, чтобы выжить в водном растворе более нескольких миллисекунд. Фактическая структура, показанная спектроскопическими исследованиями, является результатом быстрого образования полукеталя между 6-ОН и 3-карбонильными группами. Также наблюдается гидратация 2-карбонила[4]. Обычно считается, что время жизни стабилизированных видов составляет около 6 минут в биологических условиях[5]. Разрушение происходит в результате необратимого гидролиза сложноэфирной связи с последующими дополнительными реакциями разложения[6]. Кристаллизация растворов ДГК дает структуру пентациклического димера неопределенной стабильности. Повторное использование аскорбата путем активного транспорта ДГК в клетки с последующим восстановлением и повторным использованием снижает неспособность людей синтезировать его из глюкозы[7].
Транспорт в митохондрии
[править | править код]Витамин С накапливается в митохондриях, где вырабатывается большая часть свободных радикалов, поступая в виде ДГК через переносчик глюкозы GLUT10. Аскорбиновая кислота защищает митохондриальный геном и мембрану[8].
Транспорт в мозг
[править | править код]Витамин С не попадает из кровотока в головной мозг, хотя мозг является одним из органов, в которых содержится наибольшая концентрация витамина С. Вместо этого ДГК транспортируется через гематоэнцефалический барьер с помощью транспортеров GLUT1, а затем снова превращается в аскорбат[9].
Использование
[править | править код]Дегидроаскорбиновая кислота используется в качестве пищевой добавки с витамином С[10].
В качестве косметического ингредиента дегидроаскорбиновая кислота используется для улучшения внешнего вида кожи[11]. Его можно использовать в процессе перманентной завивки волос[12] и в процессе автозагара кожи[13].
В среде для выращивания клеточных культур дегидроаскорбиновая кислота использовалась для обеспечения поглощения витамина С типами клеток, которые не содержат переносчиков аскорбиновой кислоты[14].
Некоторые исследования показали, что введение дегидроаскорбиновой кислоты в качестве фармацевтического агента может обеспечить защиту от повреждения нейронов после ишемического инсульта[15]. В литературе содержится много сообщений о противовирусных эффектах витамина С[16], и одно исследование предполагает, что дегидроаскорбиновая кислота обладает более сильным противовирусным действием и другим механизмом действия, чем аскорбиновая кислота[17]. Было показано, что растворы в воде, содержащие аскорбиновую кислоту и ионы меди и/или пероксид, что приводит к быстрому окислению аскорбиновой кислоты в дегидроаскорбиновую кислоту, обладают сильными, но кратковременными антимикробными, противогрибковыми и противовирусными свойствами и используются для лечения гингивита., пародонтоз и зубной налет[18][19]. Фармацевтический продукт под названием Аскоксал является примером такого раствора, используемого для полоскания рта в качестве перорального муколитического и профилактического средства против гингивита[19][20]. Раствор аскоксала также был испытан с положительными результатами в качестве средства для лечения рецидивирующего слизисто-кожного герпеса[20] и в качестве муколитического средства при острых и хронических легочных заболеваниях, таких как эмфизема, бронхит и астма, при вдыхании аэрозолей[21].
Использованная литература
[править | править код]- ↑ May, J. M. (1998). "Ascorbate function and metabolism in the human erythrocyte". Frontiers in Bioscience. 3 (4): d1—10. doi:10.2741/a262. PMID 9405334.
- ↑ Welch, R. W. (1995). "Accumulation of Vitamin C (Ascorbate) and Its Oxidized Metabolite Dehydroascorbic Acid Occurs by Separate Mechanisms". Journal of Biological Chemistry. 270 (21): 12584—12592. doi:10.1074/jbc.270.21.12584. PMID 7759506.
{{cite journal}}: Википедия:Обслуживание CS1 (не помеченный открытым DOI) (ссылка) - ↑ Lee, Y. C. (2010). "Mitochondrial GLUT10 facilitates dehydroascorbic acid import and protects cells against oxidative stress: Mechanistic insight into arterial tortuosity syndrome". Human Molecular Genetics. 19 (19): 3721—33. doi:10.1093/hmg/ddq286. PMID 20639396.
- ↑ Kerber, R. C. (2008). ""As Simple as Possible, but Not Simpler"—The Case of Dehydroascorbic Acid". Journal of Chemical Education. 85 (9): 1237. Bibcode:2008JChEd..85.1237K. doi:10.1021/ed085p1237.
- ↑ May, J. M. (1998). "Ascorbate function and metabolism in the human erythrocyte". Frontiers in Bioscience. 3 (4): d1—10. doi:10.2741/a262. PMID 9405334.
- ↑ Kimoto, E. (1993). "Analysis of the transformation products of dehydro-L-ascorbic acid by ion-pairing high-performance liquid chromatography". Analytical Biochemistry. 214 (1): 38—44. doi:10.1006/abio.1993.1453. PMID 8250252.
- ↑ Montel-Hagen, A. (2008). "Erythrocyte Glut1 triggers dehydroascorbic acid uptake in mammals unable to synthesize vitamin C". Cell. 132 (6): 1039—48. doi:10.1016/j.cell.2008.01.042. PMID 18358815.
- ↑ Lee, Y. C. (2010). "Mitochondrial GLUT10 facilitates dehydroascorbic acid import and protects cells against oxidative stress: Mechanistic insight into arterial tortuosity syndrome". Human Molecular Genetics. 19 (19): 3721—33. doi:10.1093/hmg/ddq286. PMID 20639396.
- ↑ Huang, J. (2001). "Dehydroascorbic acid, a blood–brain barrier transportable form of vitamin C, mediates potent cerebroprotection in experimental stroke". Proceedings of the National Academy of Sciences of the United States of America. 98 (20): 11720—11724. Bibcode:2001PNAS...9811720H. doi:10.1073/pnas.171325998. PMID 11573006.
- ↑ Higdon. The Bioavailability of Different Forms of Vitamin C. The Linus Pauling Institute (май 2001). Дата обращения: 10 ноября 2010. Архивировано 13 марта 2015 года.
- ↑ https://www.researchgate.net/publication/225274699
{{citation}}:|title=пропущен или пуст (справка) - ↑ US Patent 6,506,373 Архивная копия от 25 декабря 2020 на Wayback Machine (issued Jan. 14, 2003)
- ↑ U.S. Patent Application No. 10/685,073 Архивная копия от 25 декабря 2020 на Wayback Machine Publication No. 20100221203 (published Sept. 2, 2010)
- ↑ "Vitamin C antagonizes the cytotoxic effects of antineoplastic drugs". Cancer Research. 68 (19): 8031—8038. 2008. doi:10.1158/0008-5472.CAN-08-1490. PMID 18829561.
- ↑ Huang, J. (2001). "Dehydroascorbic acid, a blood–brain barrier transportable form of vitamin C, mediates potent cerebroprotection in experimental stroke". Proceedings of the National Academy of Sciences of the United States of America. 98 (20): 11720—11724. Bibcode:2001PNAS...9811720H. doi:10.1073/pnas.171325998. PMID 11573006.
- ↑ Jariwalla, R.J. & Harakeh S. (1997). Mechanisms underlying the action of vitamin C in viral and immunodeficiency disease. In L. Packer & J. Fuchs (Eds.), Vitamin C in health and disease (pp. 309—322). New York:Marcell Dekker, Inc.
- ↑ Ericsson, Sten et al. «Anti Infectant Topical Preparations.» U.S. Patent 3,065,139, filed Nov. 9, 1954 and issued Nov. 20, 1962. Дата обращения: 24 сентября 2022. Архивировано 4 марта 2016 года.
- ↑ 1 2 Fine, Daniel. «Gel composition for reduction of gingival inflammation and retardation of dental plaque.» U.S Patent 5,298,237, filed Jan.24, 1992 and issued March 29, 1994. Дата обращения: 24 сентября 2022. Архивировано 4 марта 2016 года.
- ↑ 1 2 "Topical treatment of recurrent mucocutaneous herpes with ascorbic acid-containing solution". Antiviral Res. 27 (3): 263—70. 1995. doi:10.1016/0166-3542(95)00010-j. PMID 8540748.
- ↑ "Clinical evaluation of Ascoxal: a new mucolytic agent". Anesthesia and Analgesia. 45 (5): 531—534. 1966. doi:10.1213/00000539-196645050-00003. PMID 5330913.
Дальнейшее чтение
[править | править код]- "Recycling of vitamin C by a bystander effect". J Biol Chem. 278 (12): 10128—33. 2003. doi:10.1074/jbc.M210686200. PMID 12435736.
{{cite journal}}: Википедия:Обслуживание CS1 (не помеченный открытым DOI) (ссылка)
Ссылки
[править | править код] На Викискладе есть медиафайлы по теме Дегидроаскорбиновая кислота
На Викискладе есть медиафайлы по теме Дегидроаскорбиновая кислота