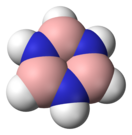
Боразол (>kjg[kl)
| Боразол | |||
|---|---|---|---|
 | |||
| Общие | |||
| Систематическое наименование |
гексагидро-1,3,5,2,4,6-триазотриборин | ||
| Традиционные названия | боразол, боразин, триборинтриимид | ||
| Хим. формула | B3N3H6 | ||
| Физические свойства | |||
| Состояние | жидкость | ||
| Молярная масса | 80.50 г/моль | ||
| Плотность | 0.81 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | −58 °C | ||
| • кипения | 55 °C | ||
| Энтальпия | |||
| • образования | -548 кДж/моль | ||
| Классификация | |||
| Рег. номер CAS | 6569-51-3 | ||
| PubChem | 138768 | ||
| Рег. номер EINECS | 641-426-2 | ||
| SMILES | |||
| InChI | |||
| ChEBI | 33119 | ||
| ChemSpider | 122374 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Боразол (боразин, триборинтриимид) — химическое вещество с химической формулой B3H6N3, бесцветная жидкость. Молекула представляет собой шестичленное плоское кольцо, в котором чередуются атомы бора и азота, каждый из них соединён с одним атомом водорода. Боразол не следует путать с борабензолом — аналогом пиридина, в котором атом азота заменён на бор.
Молекула боразола изоэлектронна молекуле бензола и имеет аналогичное строение. Уменьшение межъядерного расстояния в боразоле (d (B—N) = 0,144 нм по сравнению с одинарной связью d (B—N) = 0,154 нм) связано с делокализацией π-электронов. Распределение электронной плотности отвечает эффективным зарядам δ- и δ+ и разной полярности связей и .
Свойства
[править | править код]Являясь неорганическим аналогом бензола, боразол напоминает бензол по своим физическим свойствам (агрегатное состояние, интервал кипения, плотность и т. п.); в то же время, химические свойства боразола и бензола резко различаются.
Реакционная способность боразола выше, чем у бензола, вследствие полярности связей (три атома азота поставляют свои неподелённые электронные пары на свободные орбитали атомов бора). Так, он окисляется на воздухе, растворим в воде, с которой постепенно реагирует с образованием В(ОН)3, NH3 и Н2, и менее термически устойчив, чем бензол.
Атомы Н, связанные с атомами B, способны замещаться без разрушения цикла. Так, при действии BCl3 или BBr3 на боразол при нагревании образуются твёрдые устойчивые соединения — тригалогенборазолы B3N3H3Hal3.
Атомы H при N не способны вступать в реакции замещения.
Получение
[править | править код]- Боразол можно получить нагреванием тетрагидридобората лития и хлорида аммония:
- Реакцией трихлорида бора с хлоридом аммония и последующим восстановлением борогидридом:
- Тримеризация боразина:
Литература
[править | править код]- Карапетьянц М. Х. Дракин С. И. Общая и неорганическая химия. М.: Химия 1994
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1 (Абл-Дар). — 623 с.