5-Метил-MDA (5-Bymnl-MDA)
| 5-Метил-MDA | |
|---|---|
 | |
| Общие | |
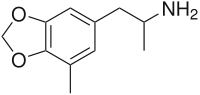
| Систематическое наименование |
1-(7-метил-1,3-бензодиоксол-5-ил)пропан-2-амин |
| Хим. формула | C11H15NO2 |
| Физические свойства | |
| Молярная масса | 193,246 г/моль |
| Классификация | |
| Рег. номер CAS | 749191-14-8 |
| PubChem | 10012829 |
| SMILES | |
| InChI | |
| ChemSpider | 8188403 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
5-Метил-3,4-метилендиоксиамфетамин (5-Метил-МДА) — энтактоген и психоделический дизайнерский наркотик класса амфетаминов. Это метилированный по кольцу гомолог MDA и структурный изомер MDMA.[1]
Эффекты и исследования
[править | править код]Исследования по различению наркотиков показали, что 5-метил-MDA заменяет MDA, MMAI и LSD, но не амфетамин, что позволяет предположить, что он производит смесь энтактогенных и галлюциногенных эффектов без каких-либо стимулирующих эффектов.
5-Метил-MDA действует как селективный агент высвобождения серотонина (SSRA) со значениями IC50 107 нМ, 11 600 нМ и 1 494 нМ для оттока серотонина, дофамина и норадреналина.[1] Он более чем в 5 раз более эффективен, чем MDA в анализах in vitro, при этом подходящая активная доза in vivo, возможно, составляет около 15–25 мг.[1] Однако последующее тестирование in vivo показало, что он не так эффективен, как считалось ранее, и активен при дозировке не менее 100 мг. 2-Метил-MDA также намного эффективнее MDA, но не настолько эффективен, как 5-метил-MDA.[1] 6-метил-MDMA (также известный как Мадам-6) в основном неактивен, вероятно, из-за стерических препятствий.[1][2]
Недавние исследования использовали данные по 2-метил-МДА и 5-метил-МДА для помощи в компьютерном моделировании комплекса переносчика серотонина.[3]
Примечания
[править | править код]- ↑ 1 2 3 4 5 Parker MA, Marona-Lewicka D, Kurrasch D, Shulgin AT, Nichols DE. Synthesis and pharmacological evaluation of ring-methylated derivatives of 3,4-(methylenedioxy)amphetamine (MDA) (англ.). — Journal of Medicinal Chemistry, 1998. — 1001-1005 p. — doi:10.1021/jm9705925.
- ↑ Shulgin A, Shulgin A. PiHKAL: A Chemical Love Story (англ.). — 1991.
- ↑ Crystal C. Walline, David E. Nichols, F. Ivy Carroll, Eric L. Barker. Comparative molecular field analysis using selectivity fields reveals residues in the third transmembrane helix of the serotonin transporter associated with substrate and antagonist recognition // The Journal of pharmacology and experimental therapeutics. — 2008-06. — Т. 325, вып. 3. — С. 791–800. — ISSN 0022-3565. — doi:10.1124/jpet.108.136200. Архивировано 13 апреля 2024 года.