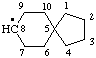Углеводородный радикал (Rilyfk;kjk;udw jg;ntgl)
Углеводоро́дный радика́л (от лат. radix «корень»), также углеводоро́дный оста́ток в химии — группа атомов, соединённая с функциональной группой молекулы. Обычно при химических реакциях радикал переходит из одного соединения в другое без изменения. Но радикал и сам может содержать функциональные группы, поэтому с его «неизменностью» нужно быть осторожным: например, аминокислота аспарагиновая кислота содержит в той части молекулы, которая в общем виде рассматривается как остаток аминокислоты, ещё одну карбоксильную группу. Часто углеводородный радикал называют просто радикал, что может вызвать путаницу с понятием свободного радикала. Некоторые углеводородные радикалы могут также являться функциональными группами, например, фенил (−C6H5), винил (−C2H3) и др. Углеводородными радикалами обычно являются остатки углеводородов, которые входят в состав многих органических соединений.
Номенклатура
[править | править код]Моновалентные углеводородные радикалы
[править | править код]Название углеводородного радикала образуется от корня названия углеводорода путём прибавления к нему суффикса -ил. Суффиксы «-ен» и «-ин» сохраняются, чтобы не потерять представление о насыщенности углеводородного радикала. В более сложных углеводородных радикалах, например, полициклических, суффикс «-ан» сохраняется[1], вероятно, ввиду большей благозвучности. Перед суффиксом «-ил» указывается порядковый номер того атома углерода от начала цепи углеродных атомов радикала, у которого есть свободная валентность — кроме случая, если свободной валентностью обладает первый атом в цепи. Нумерация цепи идёт от конца, ближайшего к свободной валентности. В случае, если в углеродной цепи с одной стороны атома со свободной(-ыми) валентностью(-ями) все атомы водорода замещены, то атом со свободными валентностями считается первым в цепи. Ранее использовался и в тривиальных названиях используется характер атома со свободной валентностью — первичный, вторичный (сек- или втор-), третичный (терц- или трет-) (см. далее). В тривиальных наименованиях используются также корни исторически сложившихся названий веществ или связанных с ними понятий. Например:
- −CH3 — метил (метан + -ил)
- −C2H5 — этил (этан + -ил)
- -CH2-CH=CH-CH3 — бут-2-енил
- Вверху изображён спиро[4.5]декан-8-ил.
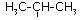 — проп-2-ил или изопропил
— проп-2-ил или изопропил- -CH2-CH(CH3)2 — 2-метилпропил или изобутил
- -CH(CH3)-CH2-CH3 — бут-2-ил или сек-бутил, или втор-бутил
- −C6H5 — фенил (фен[2] + -ил)
- -CH=CH2 — винил[3]
Поливалентные углеводородные радикалы
[править | править код]Если радикал способен присоединиться к атому углерода с образованием двойной или тройной связи или присоединиться сразу к нескольким атомам углерода (т. е., имеет несколько свободных валентностей), он называется поливалентным (в конкретном случае — би-, тривалентным, и т. д.). Названия таких радикалов строятся путём присоединения к корню названия углеводорода суффикса «-илиден» или «-илидин» соответственно. Ранее исключениями из этого правила были метилен и метин (но не теперь); впрочем, применяются и эти названия.
l-соглашение
[править | править код]Поливалентные углеводородные радикалы также могут быть поименованы согласно l-соглашению. В этом случае название строится по схеме: [заместитель при атоме со свободной валентностью] — [порядковый номер атома со свободной валентностью] ln — [название углеводорода, который получился бы при образовании на месте свободных валентностей связей с атомами водорода]. n здесь — количество свободных валентностей, которыми обладает атом.
Примеры
[править | править код]- >CH-CH3 — этилиден
- >C6H4 — фенилиден (есть 3 изомера: «1,2-», «1,3-» и «1,4-», или орто-, мета- и пара-)
- Справа внизу показан 6-аминил-бицикло[2.2.2]окт-4-ен-2-илиден или 6-аминил-2l2-бицикло[2.2.2]окт-4-ен

Обозначение в формулах
[править | править код]Если не принципиально, какой углеводородный радикал находится в молекуле, то часто его обозначают просто буквой R (например, общая формула гомологического ряда спиртов — R−OH). Иногда вместо R используют символ Org. Если соединение содержит несколько разных радикалов, их обозначают R, R', R'', R4 и т. д.
Иногда необходимо разделить ароматические, гетероциклические и алкильные радикалы. Для этого вместо символа R используют:
- для алифатических (алкил) — Alk[4] или Ak[5]
- для ароматических (арил) — Ar[4][5][6]
- для гетероциклических (гетероарил) — Het[4] или Har[5]
В органической химии нередко применяют сокращенные обозначения:
- Насыщенные углеводородные радикалы:
- Метил — Me[5][6][7], например, метанол MeOH
- Этил — Et[5][6][7], например, диэтиловый эфир Et2O
- Пропил — Pr[5][6][7], например, (N,N-дипропил)-аминопропан (трипропиламин)
- Изопропил — i-Pr[5], например, изопропилбензол
- Бутил — Bu[5][6][7]
- трет-бутил — t-Bu[5]
- Пентил — Pe[5][7]
- Гексил — Hx[5][7]
- Гептил — Hp[7]
- Октил — Oc[5][7]
- Нонил — Nn[7]
- Ненасыщенные углеводородные радикалы:
- Циклические углеводородные радикалы (циклоалкилы):
- Адамантил — Ad[8] или Adm[5]
- Циклогексил — Cy[6]
- Циклопентадиенил — Cp[6][8]
- Ароматические углеводородные радикалы (арилы):
- Полициклические ароматические углеводородные радикалы (полициклические арилы):
- Антраценил — An[5]
- Пиренил — Pyr[5]
- Периленил — Per[5]
- Тетраценил — Tet[5]
- Нафтил — Nh[5]
- Гетероциклические углеводородные радикалы (гетероарилы):
- Сульфонилы:
- Метилсульфонил (мезил) — Ms[6]
- Толилсульфонил (тозил) — Ts[4][6][8] или Tos
- Трифлил (то есть, трифторметилсульфонил ) — Tf[4][6][8]
- Карбонилы:
Иногда между обозначением характера радикала (t, i, s и др.) и остальной частью названия дефис не ставят: iPr, tBu[7]. Обозначения характера радикала принято писать курсивом.
Структурные формулы некоторых примеров изображены здесь:
-
Бензил
-
Бензоил
-
Трифторсульфонил
Применение
[править | править код]Тривиальные, неноменклатурные названия многих органических соединений состоят из названия углеводородного радикала и названия атомов или групп атомов, замещающих водород, например: СН3Сl — хлористый метил, C2H5Br — бромистый этил и т. д.
Первичные, вторичные, третичные и четвертичные атомы углерода
[править | править код]Тривиальные названия радикалов, как уже сказано выше, часто основаны на характере атомов углерода в радикале. Характер атома определяется так: первичный атом связан с одним атомом углерода, вторичный — с двумя и т. д. При названии радикалов используются латинские (sec-, tert-) или русские (втор-, трет-) приставки. Первичные атомы никак не обозначаются. Если на самом конце радикала есть третичный атом, добавляют приставку изо-. Радикалы с четверичными атомами имеют приставку нео-. Разделение атомов углерода по таким критериям крайне важно при определении стабильности реагирующих органических частиц (карбкатионов, карбанионов и радикалов). Иногда этот признак обозначают символами 10, 20, 30 и 40 соответственно.
Примечания
[править | править код]- ↑ См. правила ИЮПАК на странице в Интернете. Дата обращения: 5 февраля 2009. Архивировано из оригинала 9 февраля 2015 года.
- ↑ Старое название бензола — «фен» (греч. phainō — освещаю)
- ↑ От лат. vinum (vini) — вино; винил генетически связан с винным спиртом — этанолом C2H5OH
- ↑ 1 2 3 4 5 6 7 8 9 10 11 Instructions to authors (англ.) // Chem. Heterocycl. Comp.. — 2008. — February (vol. 44, no. 2). — P. 235–241. — doi:10.1007/s10593-008-0019-3.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 Marvin Charton. Chapter 7. Effects of structural variation on organolithium сompounds // The Chemistry of Organolithium Compounds / Ed. by Z. Rappoport and I. Marek. — John Wiley & Sons, Ltd., 2004. — Т. 1. — С. 268. — 1400 с. — ISBN 0-470-84339-X.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 Guidelines for Authors (англ.). pubs.acs.org. The Journal of Organic Chemistry (2016). Дата обращения: 24 декабря 2016. Архивировано 16 сентября 2016 года.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 Nomenclature of Lipids. Appendixes A-C (англ.). http://www.chem.qmul.ac.uk. IUPAC. Дата обращения: 24 декабря 2016. Архивировано 16 апреля 2017 года.
- ↑ 1 2 3 4 5 6 7 8 9 M.L. Waters, W.D. Wulff. Chapter 2. The Synthesis of Phenols and Quinones via Fischer Carbene Complexes // Organic Reactions / L. E. Overman (Editor-in-Chief). — John Wiley & Sons, Inc., 2008. — Т. 70. — С. 226. — 656 с. — ISBN 978-0-470-25453-0.