Водородно-калиевая аденозинтрифосфатаза (Fk;kjk;uk-tglnyfgx g;yuk[numjnskvsgmg[g)
| Н+/К+-АТФа́за | |
|---|---|
| Другие названия: | Водородно-калиевая аденозинтрифосфатаза, протонная помпа, протонный насос |
| Генетические данные | |
| Код гена: | GO:8900[1] |
| Структура и функция белка | |
| Тип белка: | гидролаза |
| Функции: | продукция соляной кислоты |
| Database Links | |
| Шифр КФ: | 7.2.2.19 |
- Статья посвящена Н+/К+-АТФазе слизистой оболочки желудка.
Водоро́дно-ка́лиевая аденозинтрифосфата́за (другие названия: Н+/К+-АТФа́за, Н+/K+-аденозинтрифосфата́за, ка́лий-водоро́дная аденозинтрифосфата́за) — фермент класса транслоказ (КФ 7.2.2.19 Архивная копия от 19 сентября 2003 на Wayback Machine). В гастроэнтерологии и фармацевтике, ориентированной на органы пищеварения, вместо водородно-калиевая аденозинтрифосфатаза обычно используют синонимы: прото́нная по́мпа, прото́нный насо́с, прото́новый насо́с, или прото́новая по́мпа (особенно часто в словосочетаниях типа: «ингибитор протонного насоса», «ингибитор протонной помпы» и т. д.).
Впервые идентифицирована в 1973 году A. Ganser и J. Forte при изучении кислотопродуцирующих клеток лягушки-быка[2].
Функции и местонахождение
[править | править код]Водородно-калиевая аденозинтрифосфатаза является протонной помпой (синоним протонным насосом) и играет важнейшую роль при секреции соляной кислоты в желудке. Н+/К+-АТФаза составляют большинство из молекул белков апикальных (направленных в просвет желудка) мембран париетальных клеток. Основная функция этих клеток заключается в продуцировании соляной кислоты (а также внутреннего фактора Кастла). Париетальные (синоним обкладочные) клетки располагаются в фундальных железах желудка. Фундальные (синоним главные) железы составляют основную часть желёз области дна, тела и интермедиальной зоны желудка и практически отсутствуют в кардиальной и пилорической частях желудка.
Структура Н+/К+-АТФазы
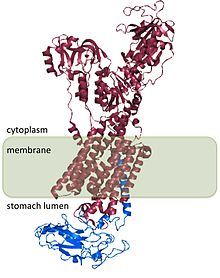
[править | править код]Н+/К+-АТФаза состоит из двух субъединиц, α (ATP4A) и β (ATP4B). Субъединица α представляет собой полипептидную цепь из 1033 аминокислотных остатков, десять раз пересекающую мембрану клетки, образующую, таким образом, пять петель, выходящих за пределы клетки. Оба конца α-субъединицы, N и С, находятся внутри клетки. Большой участок полипептидной цепи (примерно 800 аминокислотных остатков), находящийся на цитоплазматической стороне от мембраны, образует домен, являющийся каталитическим центром гидролазы.
Субъединица β является гликопротеином, содержащим 291 аминокислотный остаток, а также углеводные цитоплазматические фрагменты (примерно треть массы субъединицы) и не участвует непосредственно в процессе транспорта ионов. Полипептидная цепь этой субъединицы пересекает мембрану только один раз. N-конец этой субъединицы находится внутри париетальной клетки, в её цитоплазме, C-конец и большая часть — с внешней стороны мембраны. Эта субъединица играет важную роль в доставке вновь синтезированной субъединицы к мембране.
Продукция соляной кислоты
[править | править код]Н+/К+-АТФаза относится к большой группе белков — АТФаз, отвечающих за транспорт ионов (в большинстве случаев катионов) через клеточные мембраны практически всех биологических видов. Н+/К+-АТФаза транспортирует ион водорода Н+ из цитоплазмы париетальной клетки в полость желудка через апикальную мембрану в обмен на ион калия К+, который она переносит внутрь клетки. При этом оба катиона транспортируются против электрохимического градиента. Источником энергии для этого транспорта служит гидролиз молекулы АТФ. Одновременно с ионами водорода в просвет желудка путём активного транспорта против градиента переносятся ионы хлора Cl−. Входящие в клетку ионы К+ покидают её по градиенту концентрации вместе с ионами Cl− через апикальную мембрану париетальных клеток. Протоны Н+ образуются в эквивалентных количествах с НСО3− при диссоциации угольной кислоты Н2СО3 при участии фермента карбоангидразы. Ионы НСО3− пассивно перемещаются в кровь по градиенту концентрации через базолатеральную мембрану в обмен на Cl−. Таким образом в просвет желудка при участии Н+/К+-АТФазы выделяется соляная кислота в виде ионов Н+ и Cl−, а ионы К+ возвратным образом перемещаются через мембрану.
Ингибирование Н+/К+-АТФазы
[править | править код]Уменьшение продукции соляной кислоты в желудке является распространёнными и эффективным методом лекарственной терапии кислотозависимых заболеваний пищевода, желудка и двенадцатиперстной кишки, таких как: гастроэзофагеальная рефлюксная болезнь, диспепсии, пищевода Барретта, язвы желудка, язвы двенадцатиперстной кишки, хронического гастрита, дуоденита. Для торможения процессов кислотопродукции используют два класса лекарственных препаратов: блокаторы H2-гистаминовых рецепторов (класс АТХ А02ВA) и ингибиторы протонного насоса (класс АТХ А02ВС).
Ингибирование (торможение) продукции соляной кислоты блокаторами H2-рецепторов происходит опосредованно. Стимуляция H2-гистаминовых рецепторов периетальной клетки гистамином является необходимым условием для последующего секретирования соляной кислоты. Гистамин, воздействуя на Н2-рецепторы, что приводит к активизации аденилатциклазной системы с образованием циклического аденозинмонофосфата (цАМФ). Последний выступает в роли вторичного посредника секреции соляной кислоты. Блокаторы H2-рецепторов конкурентным образом ингибируют H2-рецепторы, уменьшая, таким образом, продукцию соляной кислоты.
Ингибиторы протонного насоса непосредственно воздействуют на Н+/К+-АТФазу. Накапливаясь в кислой среде секреторных канальцев париетальной клетки в непосредственной близости к молекуле-мишени — Н+/К+-АТФазе, они претерпевают ряд изменений — протонирование и превращение в сульфенамид. В этой форме они образуют прочные ковалентные связи с Н+/К+-АТФазой, в результате чего последняя перестаёт выполнять свои функции протонного насоса. Для того чтобы париетальная клетка вновь начала секрецию кислоты, необходим синтез новых Н+/К+-АТФаз, свободных от связи с ингибитором. Продолжительность эффекта воздействия ингибиторов протонной помпы обусловлена скоростью обновления Н+/К+-АТФаз (известно, что половина Н+/К+-АТФаз обновляется в клетке за 30-48 часов, а полностью — за 72-96 часов[3]).
См. также
[править | править код]- Натрий-калиевая аденозинтрифосфатаза (Na+/К+-АТФаза)
- Кальциевая аденозинтрифосфатаза[англ.] (Ca2+-АТФаза)
- Париетальная клетка
- Кислотность желудочного сока
- Ионные каналы
- ATP12A - каталитическая α субъединица «нежелудочной» H+/K+ АТФазы
Примечания
[править | править код]- ↑ Gene Ontology. H+/K+-exchanging ATPase. Архивная копия от 19 октября 2011 на Wayback Machine
- ↑ Бельмер С. В. Медикаментозная коррекция кислотозависимых состояний. (недоступная ссылка) Доктор. Ру, 2004, № 6.
- ↑ Яковенко А. В. рН-метрия в клинической практике. Архивная копия от 28 августа 2007 на Wayback Machine Учебно-методическое пособие. Федеральный гастроэнтерологический центр МЗ РФ, 2001, 35 с.
Ссылки
[править | править код]- BRENDA. The Comprehensive Enzyme Information System. Entry of H+/K±exchanging ATPase (EC-Number 3.6.3.10) Архивная копия от 19 октября 2011 на Wayback Machine
- Биохимия мембран. Н+/К±АТФаза слизистой желудка.
- Лопина О. Д., Котлобай А. А., Рубцов А. М. Молекулярные механизмы регуляции секреции соляной кислоты слизистой оболочки желудка. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 1997, № 6, с. 15-19.
- Статья англоязычной Википедии en:Hydrogen potassium ATPase.