Аллостерический модулятор (Gllkvmyjncyvtnw bk;rlxmkj)

В фармакологии и биохимии аллостерические модуляторы представляют собой группу веществ, которые связываются с рецептором, чтобы изменить реакцию этого рецептора на стимул. Некоторые из них, такие как бензодиазепины, являются наркотиками[1]. Сайт, с которым связывается аллостерический модулятор (то есть аллостерический сайт), отличается от того, с которым связывался бы эндогенный агонист рецептора (то есть ортостерический сайт). Модуляторы и агонисты могут быть названы лигандами рецепторов[2].
Аллостерические модуляторы могут быть 1 из 3 типов: положительные, отрицательные или нейтральные. Положительные типы усиливают реакцию рецептора за счет увеличения вероятности того, что агонист свяжется с рецептором (то есть аффинность), увеличения его способности активировать рецептор (то есть эффективности) или того и другого. Отрицательные типы снижают аффинность и/или эффективность агонистов. Нейтральные типы не влияют на активность агонистов, но могут мешать другим модуляторам связываться с аллостерическим сайтом. Некоторые модуляторы также действуют как аллостерические агонисты[3].
Термин «аллостерический» происходит от греческого языка. Allos означает «другой», а stereos — «твердый» или «форма». Это можно перевести как «другая форма», что указывает на конформационные изменения внутри рецепторов, вызванные модуляторами, посредством которых модуляторы влияют на функцию рецептора[4].
Введение
[править | править код]Аллостерические модуляторы могут изменять сродство и эффективность других веществ, действующих на рецептор. Модулятор также может повышать аффинность и снижать эффективность или наоборот[5]. Аффинность — это способность вещества связываться с рецептором. Эффективность — это способность вещества активировать рецептор, выраженная в процентах от способности вещества активировать рецептор по сравнению с эндогенным агонистом рецептора. Если эффективность равна нулю, вещество считается антагонистом[6].

Сайт, с которым связываются эндогенные агонисты, называется ортостерическим сайтом. Модуляторы не привязываются к этому сайту. Они связываются с любыми другими подходящими сайтами, которые называются аллостерическими сайтами[3]. При связывании модуляторы обычно изменяют трехмерную структуру (то есть конформацию) рецептора. Это часто приводит к изменению ортостерического сайта, что может изменить эффект связывания агониста[7]. Аллостерические модуляторы также могут стабилизировать одну из нормальных конфигураций рецептора[8].
На практике модуляция может быть сложной. Модулятор может функционировать как частичный агонист, что означает, что ему не нужен агонист, который он модулирует, для получения агонистических эффектов[9]. Кроме того, модуляция может неодинаково влиять на сродство или эффективность различных агонистов. Если группа разных агонистов, которые должны оказывать одинаковое действие, связывается с одним и тем же рецептором, некоторые модуляторы могут модулировать агонисты по-разному[10].
Классы
[править | править код]Модулятор может иметь 3 эффекта внутри рецептора. Одним из них является его способность или неспособность активировать рецептор (2 возможности). Двумя другими являются агонистическая аффинность и эффективность. Их можно увеличить, уменьшить или оставить без изменений (3 и 3 возможности). Это дает 17 возможных комбинаций модуляторов[10]. Их 18 (=2*3*3), если также включен нейтральный тип модулятора.
По всем практическим соображениям эти комбинации можно обобщить только на 5 классов[5] и 1 нейтральный:
- положительные аллостерические модуляторы (PAM) повышают аффинность и/или эффективность агонистов[7]. Клиническими примерами являются бензодиазепины, такие как диазепам, алпразолам и хлордиазепоксид, которые модулируют ГАМК- А -рецепторы, и цинакалцет, который модулирует рецепторы, чувствительные к кальцию[11].
- отрицательные аллостерические модуляторы (NAM) снижают аффинность и/или эффективность агонистов[5].Маравирок — это лекарство, которое модулирует CCR5 . Фенобам, разеглурант и дипраглурант являются экспериментальными модуляторами GRM5[11].
- Агонисты NAM работают так же, как NAM, но также как агонисты с агонистами, которые они модулируют, и без них[5].
- нейтральные аллостерические модуляторы не влияют на активность агонистов, но связываются с рецептором и предотвращают связывание PAM и других модуляторов с одним и тем же рецептором, тем самым подавляя их модуляцию[5]. Нейтральные модуляторы также называют молчащими аллостерическими модуляторами (SAM)[12] или нейтральными аллостерическими лигандами (NAL). Примером может служить 5-метил-6-(фенилэтинил)-пиридин (5MPEP), исследовательский химикат, который связывается с GRM5[13].
Механизмы
[править | править код]Из-за разнообразия мест на рецепторах, которые могут служить сайтами для аллостерической модуляции, а также из-за отсутствия окружающих их регуляторных сайтов, аллостерические модуляторы могут действовать по широкому кругу механизмов.
Модулирующая привязка
[править | править код]Некоторые аллостерические модуляторы вызывают конформационные изменения в их рецепторе-мишени, что увеличивает аффинность связывания и/или эффективность агониста рецептора[3]. Примеры таких модуляторов включают бензодиазепины и барбитураты, которые являются положительными аллостерическими модуляторами рецептора ГАМКА. Бензодиазепины, такие как диазепам, связываются между субъединицами α и γ ионных каналов рецептора ГАМКА и увеличивают частоту открытия канала, но не продолжительность каждого открытия. Барбитураты, такие как фенобарбитал, связывают β-домены и увеличивают продолжительность каждого открытия, но не частоту[14].
Модулирующая отвязка
[править | править код]
Некоторые модуляторы стабилизируют конформационные изменения, связанные с состоянием связи с агонистом. Это увеличивает вероятность того, что рецептор будет находиться в активной конформации, но не предотвращает его обратное переключение в неактивное состояние. При более высокой вероятности пребывания в активном состоянии рецептор дольше будет связываться с агонистом. Рецепторы AMPA, модулированные анирацетамом и CX614, будут дезактивироваться медленнее и способствовать более полному переносу катионов. Это, вероятно, достигается за счет связывания анирацетама или CX614 с задней частью «раковины моллюска», которая содержит сайт связывания глутамата, стабилизируя закрытую конформацию, связанную с активацией рецептора AMPA[14][15].
Предотвращение десенсибилизации
[править | править код]Общий сигнал можно увеличить, предотвратив десенсибилизацию рецептора. Десенсибилизация предотвращает активацию рецептора, несмотря на присутствие агониста. Это часто вызвано повторяющимся или интенсивным воздействием агониста. Устранение или уменьшение этого явления увеличивает общую активацию рецептора. Рецепторы AMPA восприимчивы к десенсибилизации за счет разрушения интерфейса димера лиганд-связывающего домена. Было показано, что циклотиазид стабилизирует этот интерфейс и замедляет десенсибилизацию, поэтому он считается положительным аллостерическим модулятором[15].
Стабилизация активной/неактивной конформации
[править | править код]Модуляторы могут напрямую регулировать рецепторы, а не влиять на связывание агониста. Подобно стабилизации связанной конформации рецептора, модулятор, действующий в этом механизме, стабилизирует конформацию, связанную с активным или неактивным состоянием. Это увеличивает вероятность того, что рецептор будет соответствовать стабилизированному состоянию и соответствующим образом модулировать активность рецептора. Кальций-чувствительные рецепторы можно модулировать таким образом, регулируя рН. Более низкий рН повышает стабильность неактивного состояния и тем самым снижает чувствительность рецептора. Предполагается, что изменения зарядов, связанные с регулировкой pH, вызывают конформационные изменения в рецепторе, способствующие инактивации[16].
Взаимодействие с агонистами
[править | править код]Модуляторы, повышающие только аффинность частичных и полных агонистов, позволяют быстрее достичь максимума эффективности при более низких концентрациях агонистов, то есть наклон и плато кривой доза-реакция смещаются в сторону более низких концентраций[10].
Модуляторы, повышающие эффективность, повышают максимальную эффективность частичных агонистов. Полные агонисты уже полностью активируют рецепторы, поэтому модуляторы не влияют на их максимальную эффективность, но несколько сдвигают кривую их реакции в сторону более низких концентраций агонистов[10].
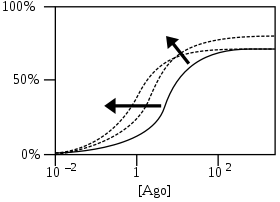
- Процент ответа рецептора в зависимости от логарифмической концентрации агониста
-
PAMs смещают начальную кривую ответа на агонист (сплошная кривая) в сторону более низких концентраций агониста за счет увеличения аффинности и/или увеличивают максимальный ответ за счет повышения эффективности. Пунктирные кривые - это 2 примера из многих возможных кривых после добавления PAM. Стрелки показывают приблизительное направление сдвигов в кривых[17].
-
PAM-агонисты работают так же, как PAMs, но сами являются агонистами. Таким образом, они вызывают ответную реакцию даже при минимальных концентрациях модулируемых ими агонистов[5].
-
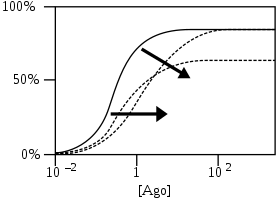
PAM-антагонисты увеличивают сродство к агонистам и сдвигают их кривые в сторону более низких концентраций, но поскольку они действуют как антагонисты, они также снижают максимальные ответы[5].
-
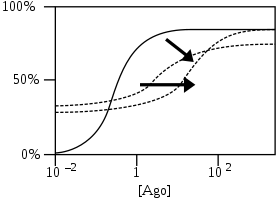
NAMs смещают кривые в сторону более высоких концентраций за счет уменьшения сродства и/или более низких максимальных реакций за счет снижения эффективности. Если сравнивать с PAMs, то эффекты NAMs обратны[5].
-
NAM-агонисты работают так же, как NAMs, но сами являются агонистами. Таким образом, они вызывают ответную реакцию даже при минимальных концентрациях модулируемых ими агонистов[5].
Медицинское значение
[править | править код]Преимущества
[править | править код]Родственные рецепторы имеют ортостерические сайты, которые очень похожи по структуре, поскольку мутации в этом сайте могут особенно снижать функцию рецептора. Это может быть вредно для организмов, поэтому эволюция часто не благоприятствует таким изменениям. Аллостерические сайты менее важны для функции рецептора, поэтому они часто имеют большие различия между родственными рецепторами. Вот почему, по сравнению с ортостерическими препаратами, аллостерические препараты могут быть очень специфичными, то есть воздействовать только на очень ограниченный набор типов рецепторов. Однако такая изменчивость аллостерических сайтов наблюдается и между видами, поэтому эффекты аллостерических препаратов сильно различаются между видами[18].
Модуляторы не могут полностью включать или выключать рецепторы, поскольку действие модуляторов зависит от эндогенных лигандов, таких как нейротрансмиттеры, производство которых в организме ограничено и контролируется. Это может снизить риск передозировки по сравнению с ортостерическими препаратами аналогичного действия. Это также может позволить использовать стратегию, при которой дозы, достаточно большие для насыщения рецепторов, можно безопасно принимать для продления действия препарата[10]. Это также позволяет рецепторам активироваться в заданное время (то есть в ответ на стимул) вместо того, чтобы постоянно активироваться агонистом, независимо от времени или цели[19].
Модуляторы влияют на существующие реакции в тканях и могут обеспечивать нацеливание лекарств на ткани. Это отличается от ортостерических препаратов, которые, как правило, оказывают менее целенаправленное воздействие в организме на все рецепторы, с которыми они могут связываться[7].
Также было показано, что некоторые модуляторы не обладают десенсибилизирующим эффектом, который имеют некоторые агонисты. Никотиновые ацетилхолиновые рецепторы, например, быстро десенсибилизируются в присутствии агонистов, но сохраняют нормальную функцию в присутствии PAM[20].
Приложения
[править | править код]Аллостерическая модуляция продемонстрировала свою пользу при многих состояниях, которые ранее было трудно контролировать с помощью других фармацевтических препаратов. Это включает:
- уменьшение негативных симптомов (дефицитов), связанных с шизофренией, с помощью экспериментальных mGluR5 -положительных модуляторов, таких как 4-нитро- N- (1,3-дифенил- 1H -пиразол-5-ил)бензамид (VU-29)[21].
- снижение беспокойства за счет положительного модулирования ГАМК-рецепторов[14].
- снижение интенсивности нарушений сна за счет положительной регуляции ГАМК-рецепторов[14].
- уменьшение депрессивных симптомов большого депрессивного расстройства и шизофрении за счет положительной модуляции дофаминовых рецепторов. Примеры включают DETQ, DPTQ и LY3154207, которые являются экспериментальными положительными модуляторами рецептора D1[22].
См. также
[править | править код]- Аллостерическая регуляция
- Положительный аллостерический модулятор рецептора AMPA
- Положительный аллостерический модулятор рецептора ГАМКА
- Отрицательный аллостерический модулятор рецептора ГАМКА
Приложения
[править | править код]- ↑ H. P. Rang. Rang and Dale's pharmacology. — Eighth edition. — [United Kingdom], 2016. — xv, 760 pages с. — ISBN 978-0-7020-5362-7, 0-7020-5362-7, 978-0-7020-5363-4, 0-7020-5363-5.
- ↑ Richard R. Neubig, Michael Spedding, Terry Kenakin, Arthur Christopoulos. International Union of Pharmacology Committee on Receptor Nomenclature and Drug Classification. XXXVIII. Update on Terms and Symbols in Quantitative Pharmacology (англ.) // Pharmacological Reviews. — 2003-12. — Vol. 55, iss. 4. — P. 597–606. — ISSN 1521-0081 0031-6997, 1521-0081. — doi:10.1124/pr.55.4.4.
- ↑ 1 2 3 "International Union of Pharmacology Committee on Receptor Nomenclature and Drug Classification. XXXVIII. Update on terms and symbols in quantitative pharmacology" (PDF). Pharmacological Reviews. 55 (4): 597—606. December 2003. doi:10.1124/pr.55.4.4. PMID 14657418. Архивировано (PDF) 26 ноября 2018. Дата обращения: 16 сентября 2022.
- ↑ David L. Nelson. Lehninger principles of biochemistry. — 5th ed. — New York: W.H. Freeman, 2008. — 1 volume (various pagings) с. — ISBN 0-7167-7108-X, 978-0-7167-7108-1, 978-1-4292-0892-5, 1-4292-0892-9, 978-1-4292-2416-1, 1-4292-2416-9, 978-1-4292-1242-7, 1-4292-1242-X. Архивировано 20 января 2010 года.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 Terry P. Kenakin. Pharmacology in drug discovery and development : understanding drug response. — Second edition. — London: Academic Press, 2017. — 1 online resource с. — ISBN 978-0-12-803753-9, 0-12-803753-9.
- ↑ Rang and Dale's pharmacology. — 8th. — Elsevier, 2016. — P. 6–20. — ISBN 978-0-7020-5362-7.
- ↑ 1 2 3 Pharmacology in drug discovery and development: understanding drug response. — P. 102–119. — ISBN 978-0-12-803752-2. — doi:10.1016/B978-0-12-803752-2.00005-3.
- ↑ R. Jin. Mechanism of Positive Allosteric Modulators Acting on AMPA Receptors (англ.) // Journal of Neuroscience. — 2005-09-28. — Vol. 25, iss. 39. — P. 9027–9036. — ISSN 1529-2401 0270-6474, 1529-2401. — doi:10.1523/JNEUROSCI.2567-05.2005.
- ↑ Oligomerization and allosteric modulation in g -protein coupled receptors. — Amsterdam: Elsevier/Academic Press, 2013. — 1 online resource (xiii, 471 pages) с. — ISBN 978-0-12-394587-7, 0-12-394587-9.
- ↑ 1 2 3 4 5 Pharmacology in drug discovery and development: understanding drug response. — 2nd. — Academic Press, 2017. — P. 102–119. — ISBN 978-0-12-803752-2. — doi:10.1016/B978-0-12-803752-2.00005-3.
- ↑ 1 2 Bruce J. Melancon, Corey R. Hopkins, Michael R. Wood, Kyle A. Emmitte, Colleen M. Niswender. Allosteric Modulation of Seven Transmembrane Spanning Receptors: Theory, Practice, and Opportunities for Central Nervous System Drug Discovery (англ.) // Journal of Medicinal Chemistry. — 2012-02-23. — Vol. 55, iss. 4. — P. 1445–1464. — ISSN 1520-4804 0022-2623, 1520-4804. — doi:10.1021/jm201139r. Архивировано 20 сентября 2022 года.
- ↑ Chemokine receptor oligomerization and allostery. — 2013. — Vol. 115. — P. 4–5. — ISBN 978-0-12-394587-7. — doi:10.1016/B978-0-12-394587-7.00009-9.
- ↑ Shane D. Hellyer, Sabine Albold, Taide Wang, Amy N. Y. Chen, Lauren T. May. “Selective” Class C G Protein-Coupled Receptor Modulators Are Neutral or Biased mGlu 5 Allosteric Ligands (англ.) // Molecular Pharmacology. — 2018-05. — Vol. 93, iss. 5. — P. 504–514. — ISSN 1521-0111 0026-895X, 1521-0111. — doi:10.1124/mol.117.111518.
- ↑ 1 2 3 4 Biased signaling in physiology, pharmacology and therapeutics. — San Diego, California, 2014. — 1 online resource (317 pages) с. — ISBN 978-0-12-411507-1, 0-12-411507-1.
- ↑ 1 2 "Mechanism of Positive Allosteric Modulators Acting on AMPA Receptors". Journal of Neuroscience. 25 (39): 9027—9036. 2005-09-28. doi:10.1523/JNEUROSCI.2567-05.2005. ISSN 0270-6474. PMID 16192394.
- ↑ Principles of bone biology. — Fourth edition. — London, United Kingdom, 2020. — 1 online resource (2 volumes) с. — ISBN 9780128148419.
- ↑ Pharmacology in drug discovery and development: understanding drug response. — 2nd. — Academic Press, 2017. — P. 102–119. — ISBN 978-0-12-803752-2. — doi:10.1016/B978-0-12-803752-2.00005-3.Kenakin TP (2017). Pharmacology in drug discovery and development: understanding drug response (2nd ed.). Academic Press. pp. 102–119. doi:10.1016/B978-0-12-803752-2.00005-3. ISBN 978-0-12-803752-2.
- ↑ Shaoyong Lu, Xinheng He, Duan Ni, Jian Zhang. Allosteric Modulator Discovery: From Serendipity to Structure-Based Design (англ.) // Journal of Medicinal Chemistry. — 2019-07-25. — Vol. 62, iss. 14. — P. 6405–6421. — ISSN 1520-4804 0022-2623, 1520-4804. — doi:10.1021/acs.jmedchem.8b01749. Архивировано 20 сентября 2022 года.
- ↑ Yuanheng Li, Lilan Sun, Taoyi Yang, Wenxuan Jiao, Jingshu Tang. Design and Synthesis of Novel Positive Allosteric Modulators of α7 Nicotinic Acetylcholine Receptors with the Ability To Rescue Auditory Gating Deficit in Mice (англ.) // Journal of Medicinal Chemistry. — 2019-01-10. — Vol. 62, iss. 1. — P. 159–173. — ISSN 1520-4804 0022-2623, 1520-4804. — doi:10.1021/acs.jmedchem.7b01492. Архивировано 20 сентября 2022 года.
- ↑ Dustin K. Williams, Jingyi Wang, Roger L. Papke. Positive allosteric modulators as an approach to nicotinic acetylcholine receptor-targeted therapeutics: Advantages and limitations (англ.) // Biochemical Pharmacology. — 2011-10. — Vol. 82, iss. 8. — P. 915–930. — doi:10.1016/j.bcp.2011.05.001. Архивировано 11 октября 2022 года.
- ↑ Jennifer E Ayala, Yelin Chen, Jessica L Banko, Douglas J Sheffler, Richard Williams. mGluR5 Positive Allosteric Modulators Facilitate both Hippocampal LTP and LTD and Enhance Spatial Learning (англ.) // Neuropsychopharmacology. — 2009-08. — Vol. 34, iss. 9. — P. 2057–2071. — ISSN 1740-634X 0893-133X, 1740-634X. — doi:10.1038/npp.2009.30. Архивировано 22 сентября 2022 года.
- ↑ Neuropsychotherapeutics. — First edition. — Amsterdam, The Netherlands, 2019. — 1 online resource (312 pages) с. — ISBN 9780128166680.