Частичный агонист (Cgvmncudw gikunvm)
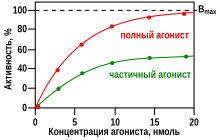


В фармакологии термин части́чные агони́сты (также употребителен термин «парциа́льные агонисты», partial agonist) применяется по отношению к лекарствам и химическим соединениям, которые являются лигандами для конкретного подтипа клеточных рецепторов (то есть связываются с ними) и способны активировать рецептор, то есть переводить его в активную пространственную конфигурацию (проявлять агонистические свойства), но с меньшей вероятностью (меньшей рецепторной эффективностью), чем эндогенный агонист тех же рецепторов, рецепторная эффективность которого принимается за 100 % и который рассматривается, таким образом, как истинный полный агонист. Другими словами, внутренняя агонистическая активность частичного агониста (синоним его «рецепторной эффективности») по определению всегда больше 0 % (иначе он был бы «нейтральным антагонистом»), но меньше 100 % (иначе он был бы «полным агонистом»).
На практике внутренняя агонистическая активность веществ, обычно рассматриваемых в качестве «частичных агонистов», как правило, выше 10—20 %, но ниже 70—80 %, поскольку «слабые» частичные агонисты (с внутренней агонистической активностью, меньшей 10—20 %) и в эксперименте, и в клинической практике обычно трудно отличимы от «истинных» нейтральных антагонистов (имеющих строго нулевую внутреннюю агонистическую активность), а «сильные» частичные агонисты (с внутренней агонистической активностью, большей 70—90 %) трудно отличимы от «истинных» полных агонистов (имеющих внутреннюю агонистическую активность, строго равную 100 %). Более того, существует, на самом деле, очень мало «истинных» нейтральных антагонистов (со строго равной нулю внутренней агонистической активностью) — большинство из них являются либо слабыми и очень слабыми частичными агонистами, либо обратными агонистами. Точно так же существует очень мало «истинных» полных агонистов (кроме эндогенного агониста, который по определению принимается за 100 %) — большинство из них являются просто сильными или очень сильными частичными агонистами. Более того, даже если в эксперименте для некоего соединения получено значение внутренней агонистической активности, строго равное 0 % или 100 %, то это вовсе не значит, что это соединение действительно является «истинным нейтральным антагонистом» или «истинным полным агонистом» — это всего лишь значит, что разница между измеренным значением и 0 % или 100 % меньше погрешности метода измерения. Таким образом, с формально-математической точки зрения, частичные агонисты являются наиболее распространённым типом экзогенных лигандов, причём в зависимости от величины внутренней агонистической активности они могут клинически рассматриваться и применяться либо в качестве квази-«антагонистов» (слабые частичные агонисты с внутренней агонистической активностью менее 10-20 % от активности эндогенного лиганда), либо в качестве квази-«полных агонистов» (сильные частичные агонисты с внутренней агонистической активностью выше 70-90 % от активности эндогенного лиганда), либо в качестве «частичных агонистов» (при промежуточных значениях внутренней агонистической активности).
Частичные агонисты также могут рассматриваться как лиганды, которые проявляют как агонистические, так и антагонистические свойства в зависимости от конкретной клинической или экспериментальной ситуации, или, иначе говоря, как «смешанные агонисты-антагонисты». А именно, когда в биологической системе присутствуют одновременно частичный агонист и полный агонист (например, эндогенный агонист) или просто более сильный частичный агонист одних и тех же рецепторов, то «более слабый» частичный агонист, на самом деле, проявляет свойства конкурентного антагониста этих рецепторов, конкурируя с «более сильным» частичным агонистом или с полным агонистом (в том числе эндогенным лигандом) за занятость рецепторов и вызывая, таким образом, общее снижение уровня активности рецепторной системы по сравнению с присутствием одного лишь только полного агониста или «более сильного» частичного агониста в той же концентрации[1]. Клиническая польза и эффективность частичных агонистов определяются тем, что они могут одновременно и активировать рецепторные системы при недостаточном уровне их стимуляции (низком уровне эндогенного полного агониста) до некоего желаемого «субмаксимального» уровня (который ниже, чем при применении полного агониста), и предотвращать чрезмерную, избыточную и вредную гиперстимуляцию рецепторов, наступающую при чрезмерно высоком уровне эндогенного агониста[2]. Способность частичных агонистов действовать как конкурентные антагонисты в присутствии полного агониста (в том числе эндогенного лиганда) или в присутствии «более сильного» частичного агониста весьма важна для клинической практики. Так, например, способность налоксона (являющегося на самом деле не истинным антагонистом, а весьма и весьма слабым частичным агонистом опиоидных рецепторов — настолько слабым, что его частичная агонистическая активность никакого клинического значения не имеет и его традиционно относят к опиоидным антагонистам) снимать проявления опиоидной интоксикации основана именно на этом свойстве. Не менее важна для клинической практики способность сильных частичных агонистов (с рецепторной эффективностью 80-90 % и выше) действовать практически неотличимо от «истинных» полных агонистов. Так, например, прессорное вещество фенилэфрин (мезатон), являющееся структурным аналогом норадреналина, является на самом деле весьма сильным, «почти полным» частичным агонистом α-адренорецепторов, а не «истинным» полным агонистом. Но это отличие настолько мало, что оно не имеет клинического значения и позволяет применять фенилэфрин в качестве «почти полного агониста», прессорного вещества для купирования гипотензии, вместо короткодействующего и неудобного для применения норадреналина. Аналогичным образом сальбутамол является сильным, «почти полным» частичным агонистом β-адренорецепторов, настолько сильным, что клинически его действие на бронхи неотличимо от действия адреналина, что и позволяет его применять в качестве бронходилататора.
Другие важные примеры лекарств, являющихся частичными агонистами тех или иных рецепторов (причём в истинном, «сбалансированном» смысле — не в смысле подобия вышеприведённым крайним примерам с налоксоном и с фенилэфрином и сальбутамолом), включают в себя небензодиазепиновый анксиолитик буспирон, атипичный антипсихотик арипипразол, частичный агонист опиоидных рецепторов наркотический анальгетик бупренорфин, метаболит клозапина норклозапин. Имеются также примеры лигандов, активирующих рецептор PPARγ именно как частичные агонисты — хонокиол и фалкариндиол[3][4].
См. также
[править | править код]Примечания
[править | править код]- ↑ Calvey, Norman; Williams, Norton. Partial agonists // Principles and Practice of Pharmacology for Anaesthetists (англ.). — 2009. — P. 62. — ISBN 978-1-4051-9484-6.
- ↑ Zhu, Bao Ting. Mechanistic explanation for the unique pharmacologic properties of receptor partial agonists (англ.) // Biomedicine & Pharmacotherapy[англ.] : journal. — 2005. — Vol. 59, no. 3. — P. 76—89. — doi:10.1016/j.biopha.2005.01.010. — PMID 15795100.
- ↑ Atanasov, Atanas G.; Wang, Jian N.; Gu, Shi P.; Bu, Jing; Kramer, Matthias P.; Baumgartner, Lisa; Fakhrudin, Nanang; Ladurner, Angela; Malainer, Clemens; Vuorinen, Anna; Noha, Stefan M.; Schwaiger, Stefan; Rollinger, Judith M.; Schuster, Daniela; Stuppner, Hermann; Dirsch, Verena M.; Heiss, Elke H. Honokiol: A non-adipogenic PPARγ agonist from nature (англ.) // Biochimica et Biophysica Acta[англ.] : journal. — 2013. — Vol. 1830, no. 10. — P. 4813—4819. — doi:10.1016/j.bbagen.2013.06.021. — PMID 23811337. — PMC 3790966.
- ↑ Atanasov, Atanas G.; Blunder, Martina; Fakhrudin, Nanang; Liu, Xin; Noha, Stefan M.; Malainer, Clemens; Kramer, Matthias P.; Cocic, Amina; Kunert, Olaf; Schinkovitz, Andreas; Heiss, Elke H.; Schuster, Daniela; Dirsch, Verena M.; Bauer, Rudolf. Polyacetylenes from Notopterygium incisum–New Selective Partial Agonists of Peroxisome Proliferator-Activated Receptor-Gamma (англ.) // PLoS ONE : journal. — 2013. — Vol. 8, no. 4. — P. e61755. — doi:10.1371/journal.pone.0061755. — . — PMID 23630612. — PMC 3632601.