ZMapp (ZMapp)
| ZMapp | |
|---|---|
| Состав | |
ZMapp — экспериментальный биологический препарат разработки США и Канады, который в августе 2014 года был представлен в качестве лекарственного средства от разразившейся в этом году в ряде стран Западной Африки эпидемической вспышки геморрагической лихорадки Эбола. Он состоит из трёх гуманизированных[a] моноклональных антител, полученных по гибридомной технологии[2][3].
Разработка
[править | править код]Созданием препарата занимается фирма Mapp Biopharmaceutical[англ.] из калифорнийского города Сан-Диего[4], правительство США и Управление здравоохранения Канады[5]. Эта разработка родилась на основе программы получения лекарственных препаратов из антител, которая уже больше десяти лет проводилась в США для защиты своих военнослужащих[6] и многолетнего финансирования управлением здравоохранения Канады[7].
Два из трёх гуманизированных моноклональных антител (англ. mAbs) в составе препарата были взяты из комбинации антител ZMAb (получена Defyrus/PHAC), а третье из MB-003 (получено Mapp)[6].
По данным авторов исследования, при экспериментальном заражении вирусом лихорадки Эбола макак-резус, в случае начала лечения данным препаратом не позднее 5 дней с момента инфицирования выживаемость животных составила 100 %, при том что до введения препарата у многих отмечались серьёзные проявления заболевания такие, как значительное повышение температуры тела, наличие вируса в крови (виремия), аномалии количества кровяных телец и биохимического состава крови. Тяжелое течение болезни, проявлявшееся в повышении количества ферментов печени, кровотечениях из слизистых оболочек и генерализованной петехии (мельчайших кровоизлияниях на коже в результате разрыва капилляров[8][9]), оказалось обратимым с полным выздоровлением животных-пациентов[2].
Производство
[править | править код]В разделе не хватает ссылок на источники (см. рекомендации по поиску). |
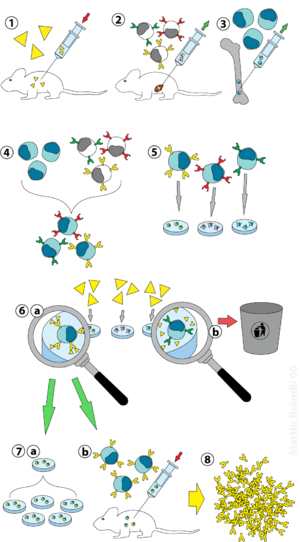
(1) иммунизация животных;
(2) выделение В-лимфоцитов из селезёнки;
(3) культура клеток миеломы;
(4) слияние В-лимфоцитов и клеток миеломы;
(5) сегрегация клеточных линий;
(6) скрининг и селекция линий, производящих антитела;
(7) размножение гибридомы in vitro (a) или in vivo (b);
(8) получение антител.
Первоначальное количество антител к вирусу получается по гибридомной технологии. При этом методе мышам вводится вирус, у них развивается иммунный ответ, из их селезёнки выделяются В-лимфоциты, которые сливаются с опухолевыми клетками — клетками миеломы, после чего производятся скрининг и селекция клеточных линий, производящих антитела, для отбора лучших антител. После отбора такого антитела выделяют ген, кодирующий его, а затем антитело гуманизируют (заменяют участки белковой цепи, свойственные животному, от которого оно получено, на свойственные человеку) во избежание аллергической реакции.
Для последующего размножения гибридомы в случае ZMapp использовались генетически-модифицируемые тем самым растения табака, которые начинали продуцировать соответствующие антитела. Модифицирование (трансфекция) генетического аппарата табачных растений производилось специально подобранным переносчиком вирусной инфекции — культурой инфицированной вирусом бактерии Agrobacterium tumefaciens, известной своей способностью внедрять участки своей ДНК в ДНК растений и поэтому важной для генной инженерии в агробиологии. Затем из растений получают нужные антитела.
Применение
[править | править код]На сайте разработчика на конец августа 2014 было указано, что препарат попал в кандидаты на то, чтобы стать лекарством от Эбола в январе того же года, но что его применение на людях ещё не разрешено американскими властями из-за неисследованности его эффективности и безопасности у человека, и что компания ещё не располагает достаточным количеством препарата[5].
В августе 2014 г. сообщалось о двух излеченных с помощью ZMapp американских медиках[10][11] (главном враче либерийского медицинского центра Samaritan’s Purse д-ре Кенте Брэнтли и помогавшей ему миссионерке Serving in Mission[англ.] (SIM) Нэнси Райтбол (англ. Dr. Kent Brantly и Nancy Writebol) из Университета Эмори в городе Атланта штата Джорджия), оказывавших помощь населению Либерии[12].
По сообщению Центра по контролю и профилактике заболеваний США, экспериментальное лечение своих добровольных сотрудников было заказано самой организацией Samaritan’s Purse, которая связалась с CDC. CDC связала заявителей с организацией «Национальные институты здравоохранения США» (англ. National Institutes of Health (NIH)), а там их связали с частной компанией — разработчиком препарата. В итоге американские государственные организации непосредственно не участвовали в проведении лечения препаратом, эффективность и безопасность которого не были доказаны, вследствие чего он ещё не получил разрешения к применению на людях в США. Там же со ссылкой на производителя было заявлено, что на тот момент получено лишь минимальное количество доз препарата и все они используются, и что заказ на новые разместить пока невозможно. Там же сказано, что согласно регламентам Управления по контролю за продуктами и лекарствами США (FDA) в исключительных случаях может допускаться применение инновационных лекарственных средств, которые ещё не прошли полного цикла клинических испытаний[13].
Заболевший доктор также получил переливание крови 14-летнего подростка, который пережил данную инфекцию под руководством этого врача и был ему благодарен[14]. При анализе наблюдений над эпидемией 1995 года выяснилось, что уже тогда жизнь 7 из 8 заболевших медиков была спасена иммунизацией с помощью переливания крови успешно переживших заболевание, но этот метод не стал общепринятым в ходе нынешней эпидемии из-за его малоизученности применительно к данному заболеванию[15].
Применение остродефицитного, но потенциально эффективного препарата для спасения жизни именно иностранцев, представителей белой расы, традиционно связывавшейся в Африке с идеями колониализма, вызвало сомнения в этичности данного шага у части общественности и вынудило президента Samaritan’s Purse подтвердить в прессе правильность сделанного выбора. Президент организации аргументировал принятое решение тем, что самоотверженный и обладающий крепкой верой в бога врач достоин излечения, за которое молились члены этой организации, к тому же излечение и отсутствие тяжелых побочных действий в силу малоисследованности препарата были не гарантированы. Инициаторов дискуссии автор ответа представил как людей, живущих в США в благополучных условиях и далеких от мысли о том, чтобы поехать в Африку для оказания реальной помощи её жителям. Он сообщил также, что существовало всего три дозы препарата, из которых две получила в Либерии г-жа Райтбол, и третью ввели врачу[16].
В 2014 году СМИ сообщали, что лечение с помощью ZMapp испанского священника, заразившегося в Либерии, оказалось безуспешным и болезнь окончилась летальным исходом[17][18].
Комментарии
[править | править код]Примечания
[править | править код]- ↑ Тарантул, 2005.
- ↑ 1 2 Qiu, Xiangguo. Reversion of advanced Ebola virus disease in nonhuman primates with ZMapp : [англ.] / Xiangguo Qiu, Gary Wong, Jonathan Audet … [et al.] // Nature : j. — 2014. — Vol. 514, no. 7520 (2 October). — P. 47–53. — doi:10.1038/nature13777. — PMID 25171469. — PMC PMC4214273.
- ↑ Невинная, Ирина. Лекарство против Эболы показало первые результаты : [арх. 9 апреля 2016] // Российская газета. — 2014. — 30 августа.
- ↑ Morin, Monte. Mystery Ebola virus serum manufactured by San Diego firm : [англ.] : [арх. 28 августа 2021] // Los Angeles Times. — 2014. — 4 August.
- ↑ 1 2 ZMapp™ Information Sheet : [англ.] : [арх. 12 августа 2014] / LeafBio. — Mapp Biopharmaceutical. — (недоступная ссылка).
- ↑ 1 2 Langreth, Robert. Ebola Drug Made From Tobacco Plant Saves U.S. Aid Workers : [англ.] : [арх. 24 января 2015] / Robert Langreth, Caroline Chen, James Nash … [et al.] // Business Week. — 2014. — 4 August.
- ↑ Branswell, Helen. Experimental Ebola drug based on research discoveries from Canada's national lab : [англ.] : [арх. 10 августа 2014] // The Brandon Sun. — 2014. — 5 August.
- ↑ Петехия // Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров. — 3-е изд. — М. : Советская энциклопедия, 1969—1978.
- ↑ Петехия // Медицинская энциклопедия : [арх. 3 сентября 2014].
- ↑ Ebola crisis : Doctors in Liberia «recovering after taking ZMapp» : [англ.] : [арх. 19 августа 2014] // BBC. — 2014. — 19 August.
- ↑ Бакланов, Александр Выздоровел заразившийся вирусом Эбола врач из США. Сноб (21 августа 2014). Дата обращения: 17 августа 2019. Архивировано 22 августа 2014 года.
- ↑ Justice, Elaine Emory University Hospital Ebola team featured by NBC News (англ.). Emory News center (3 сентября 2014). Дата обращения: 18 августа 2019. Архивировано 21 апреля 2017 года.
- ↑ Q&A on Experimental Treatments and Vaccines for Ebola. Ebola Hemorrhagic Fever (англ.). CDC. Архивировано 8 августа 2014 года.
- ↑ 'A Miraculous Day'. Dr. Kent Brantly credits God for his recovery from the Ebola virus as he is released from Emory University Hospital (англ.). Samaritan's Purse (21 августа 2014). Дата обращения: 17 августа 2019. Архивировано 16 августа 2019 года.
- ↑ Wolfson, Elijah. The 20-Year-Old Ebola Treatment That Could Save Kent Brantly : [англ.] : [арх. 8 сентября 2014] // Newsweek. — 2014. — 1 August.
- ↑ Graham, Franklin Franklin Graham: Saving Ebola doctor no ethical dilemma (англ.). USQ Today (21 августа 2014). Дата обращения: 17 августа 2019. Архивировано 6 января 2020 года.
- ↑ Бакланов, А. От лихорадки Эбола погиб третий европеец. Сноб (12 августа 2014). Дата обращения: 17 августа 2019. Архивировано 1 марта 2021 года.
- ↑ Álvarez, P. Muere el sacerdote Miguel Pajares, el primer fallecido por ébola en Europa : El cuerpo del religioso ha sido incinerado sin que se le practicase la autopsia : [исп.] : [арх. 13 августа 2014] / P. Álvarez, M. A. Torres // EL PAÍS. — 2014. — 12 agosto.
Литература
[править | править код]- Тарантул В. З. и др. Гуманизированные антитела // Словарь биотехнологических терминов. — ИНИЦ Роспатента, 2005. — 126 с.
Для улучшения этой статьи по медицине желательно:
|