N-Этилмалеимид (N-|mnlbglynbn;)
| N-Этилмалеимид | |
|---|---|
 | |
| Общие | |
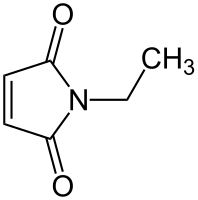
| Систематическое наименование |
1-Этилпиррол-2,5-дион |
| Сокращения | НЭМ |
| Традиционные названия | Этилмалеимид |
| Хим. формула | C6H7NO2 |
| Физические свойства | |
| Молярная масса | 125,12528 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 43-46 °C |
| • кипения | 210 °C |
| Классификация | |
| Рег. номер CAS | 128-53-0 |
| PubChem | 4362 |
| Рег. номер EINECS | 204-892-4 |
| SMILES | |
| InChI | |
| ChEBI | 44485 |
| ChemSpider | 4209 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
N-Этилмалеимид (НЭМ) — производное малеиновой кислоты. Он содержит имидную функциональную группу и представляет собой активированный алкен, который реагирует с тиолами и часто используется для модификации остатков цистеина в белках и пептидах[1].
Химические свойства
[править | править код]N-Этилмалеимид является акцептором Михаэля. Это означает, что он может присоединять нуклеофилы, такие как тиолы. Образовавшийся в результате такой реакции тиоэфир обладает очень прочной C–S-связью, и реакция является практически необратимой. Реакция протекает при рН 6,5—7,5. N-этилмалеимид может реагировать с аминами или подвергаться гидролизу при более щелочных рН. N-этилмалеимид широко использовался для определения функциональной роли тиольных групп в энзимологии. Он является необратимым ингибитором всех цистеиновых пептидаз, поскольку осуществляет алкилирование тиольных групп в активном центре (см. схему)[2][3].

Тематические исследования
[править | править код]НЭМ блокирует везикулярный транспорт. Лизисные буферы с 20—25 мМ N-этилмалеимида используются для ингибирования де-сумоилирования белков во время вестерн-блоттинга. НЭМ также используется в качестве ингибитора деубиквитинилирования.
Артур Корнберг и его коллеги использовали N-этилмалеимид, чтобы выключить ДНК-полимеразу III и сравнить её активность с ДНК-полимеразой I. Корнберг был удостоен Нобелевской премии за открытие ДНК-полимеразы I, которая в то время считалась главной полимеразой бактериальной репликации, хотя позже его сын Томас показал, что основной репликативной полимеразой у бактерий является ещё не открытая в то время ДНК-полимераза III.
N-Этилмалеимид активирует оуабаин-нечувствительное хлор-зависимое поступление ионов калия в красные кровяные тельца овец и коз[4]. Шестнадцать лет спустя это открытие способствовало открытию K+/Cl- котранспортёров в клетках человеческих эмбрионов, в которые ввели кДНК изоформы по KCC1[5]. С тех пор N-этилмалеимид широко используется в качестве диагностического инструмента для определения наличия K+/Cl- симпортов в клетках разных видов животных[6][7][8][9].
Примечания
[править | править код]- ↑ Thiol reactive probes Архивировано 28 января 2008 года. at Invitrogen
- ↑ Nelson, D. L.; Cox, M. M. "Lehninger, Principles of Biochemistry" 3rd Ed. Worth Publishing: New York, 2000.
- ↑ Gregory, J. D. (1955) J. Am. Chem.
- ↑ A chloride dependent K+ flux induced by N ethylmaleimide in genetically low K+ sheep and goat erythrocytes.
- ↑ Gillen CM, Brill S, Payne JA, Forbush B 3rd: Molecular cloning and functional expression of the K-Cl cotransporter from rabbit, rat, and human.
- ↑ Regulation of K-Cl cotransport: from function to genes.
- ↑ K+ Cl Cotransport: Sulfhydryl, divalent cations and the mechanism of volume activation in a red cell.
- ↑ . doi:10.1016/j.cell.2009.05.031.
- ↑ Jennings, M. L. & Al-Rohil, N. S. J. gen. Physiol. 95, 1021−1040, 1990
Внешние ссылки
[править | править код]- The MEROPS online database for peptidases and their inhibitors: NEM (недоступная ссылка)
- The bifunctional analogues such as p-NN'-phenylenebismaleimide can be used as cross-linking reagent for cystine residues. see Lutter, L. C., Zeichhardt, H., Kurland, C. G. & Stoffier,G. (1972) Mol. Gen. Genet. 119, 357-366.