2,4,5-Трихлорфеноксиуксусная кислота (2,4,5-Mjn]lkjsyuktvnrtvrvugx tnvlkmg)
| 2,4,5-Трихлорфеноксиуксусная кислота | |
|---|---|
  | |
| Общие | |
| Систематическое наименование |
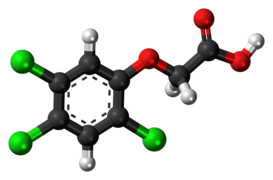
2,4,5-трихлорфеноксиуксусная кислота |
| Сокращения | 2,4,5-T |
| Хим. формула | C8H5Cl3O3 |
| Физические свойства | |
| Состояние | От беловатого до жёлтого цвета кристаллическое твёрдое вещество |
| Молярная масса | 255,48 г/моль |
| Плотность | 1,80 г/см3 при 20 °C[1] |
| Термические свойства | |
| Температура | |
| • плавления | 154-158 °C |
| • кипения | разлагается[2] °C |
| Давление пара | 1 x 10-7 мм. рт. ст.[2] |
| Химические свойства | |
| Растворимость | |
| • в воде | 278 мг·л−1 при 20 °C[1] |
| Классификация | |
| Рег. номер CAS | 93-76-5 |
| PubChem | 1480 |
| Рег. номер EINECS | 202-273-3 |
| SMILES | |
| InChI | |
| RTECS | AJ8400000 |
| ChEBI | 27903 |
| ChemSpider | 1435 |
| Безопасность | |
| Предельная концентрация |
|
| ЛД50 |
381 мг/кг (морская свинка, орально)
|
| Фразы риска (R) | R22 R36/37/38 R50/53 |
| Фразы безопасности (S) | (S2) S24 S60 S61 |
| Краткие характер. опасности (H) |
H302, H315, H319, H335, H410 |
| Меры предостор. (P) |
P261, P273, P305+351+338, P501 |
| Пиктограммы СГС |
|
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
2,4,5-Трихлорфеноксиуксусная кислота (сокращённо 2,4,5-T) — синтетический ауксин, производное феноксиуксусной кислоты. Уже сам по себе токсичный, 2,4,5-Т в процессе производства загрязнялся следовыми количествами 2,3,7,8-тетрахлордибензодиоксина (2,3,7,8-ТХДД), канцерогеном и пестицидом с долгосрочными последствиями для окружающей среды. Во время войны во Вьетнаме применялся в качестве дефолианта.
История
[править | править код]2,4,5-T попал на рынок в 1948 году. При его изготовлении происходили серьёзным аварии с выбросом диоксинов. В результате промышленной аварии на производственном заводе Монсанто в городе Нитро в 1949 году 120 работников подверглись воздействию реакционной смеси и страдали от хлоракне[англ.]. Ещё одно серьезное происшествие произошло в 1952 на заводе Boehringer Ingelheim в Hamburg Moorfleet, где ещё 30 работников заболели хлоракне. В исследованиях по оптимизации синтеза 2,4,5-T в 1968 году в британской лаборатории Coalite Chemicals взорвался реакционный сосуд, убив одного работника[5].
Во время войны во Вьетнаме 2,4,5-Т частично в виде его изопропилового и н-бутилового эфира, использовался как активный ингредиент Агента Оранж, Агента Грин, Агента Пинк и Агента Пёрпл. В этих смесях в качестве загрязнение содержалось между 0,02 и 15 мг/кг 2,3,7,8-ТХДД, который оказался там из-за несовершенства технологии производства 2,4,5-трихлорфеноксиуксусной кислоты. Количество израсходованного во время войны во Вьетнаме 2,3,7,8-ТХДД оценивается в 166 кг[6].
В период с 1971 по 1974 год специализированная компания в Миссури неправильно утилизировала маслянистые остатки производства 2,4,5-Т. Вместо дальнейшей утилизации они разбрызгивали его на ипподромах, чтобы связать пыль. Лошади очень чувствительны к диоксинам, более 50 животных погибли. Остатки смеси были распрысканы на улицах Таймс-Бич. Во время наводнения 1982 года тротуары, обработанные маслянистыми остатками, смыло в дома. Население было эвакуировано, а государство выкупило значительную часть земли[5].
Принцип действия и применение
[править | править код]2,4,5-Т, как и родственная ему 2,4-дихлорфеноксиуксусная кислота, представляют собой синтетический аналог гормонов растений из группы ауксинов. Они вызывают чрезмерно быстрый рост, который приводит к гибели растения[источник не указан 1336 дней].
В 1970-х и 1980-х годах 2,4,5-Т под торговым названием Tormona использовался против древесных растений для так называемой очистки в лесном хозяйстве. В сочетании с другими гербицидами он также применяется при выращивании зерновых культур, на пастбищах и газонах. Обычно продается в виде порошка растворимых в воде солей щелочных металлов или аммония, а также как сложные эфиры 2,4,5-T в виде концентрированных эмульсий.
В Германии использование этого гербицида запрещено с 1988 года[1], так же как в Австрии и Швейцарии[7].
Производство
[править | править код]Для изготовления этого вещества тетрахлорбензол и 2,4,5-трихлорфенол при температуре около 140 °C смешивают с хлоруксусной кислотой, в результате чего образуется 2,4,5-трихлорфеноксиуксусная кислота. Если температура резко возрастет на последней стадии реакции, образуются ядовитые диоксины.
Токсикология
[править | править код]2,4,5-T попадает в организм преимущественно через кожу или пищеварительный тракт. Он действует на слизистые оболочки и кожу, сильно их раздражая, причём этот эффект объясняется наличием в препарате 2,3,7,8-ТХДД. После приема внутрь общее состояние здоровья ухудшается. Вещество повреждает нервную и сердечно-сосудистую систему. У добровольцев, которые принимали 2,4,5-Т в дозах до 5 мг/кг массы тела, не обнаруживалось никаких клинических симптомов. Они сообщили лишь о металлическом привкусе во рту. В исследованиях на животных полулетальная доза (ЛД50) составила 100 мг/кг массы тела для собак, 500 мг/кг для крыс и около 800 мг/кг для мышей[1]. В проведенных исследованиях по хронической токсичности в большинстве случаев не отслеживалось, в какой мере 2,4,5-Т был загрязнён диоксинами. В экспериментах на животных хроническое воздействие приводило к повреждению печени и почек. Допустимая суточная доза для человека была установлена на уровне 0,03 мг/кг массы тела. Предполагается, что чистая 2,4,5-трихлорфеноксиуксусная кислота не обладает тератогенными, мутагенными или канцерогенными свойствами[1].
В среднем 2,4,5-Т содержит около 10 миллионных долей диоксинов[5].
Воздействия на окружающую среду
[править | править код]Соединение разлагалось в растениях после удаления остатка уксусной кислоты путем гидроксилирования бензольного кольца. Время сохранения в почве после применения 1,5 кг 2,4,5-Т на га оценивается в 2 месяца. Гербицид был классифицирован как нетоксичный для пчёл. LC50 для радужной форели для эфиров препарата была определена в 12 мг при длительности воздействия 24 часа[8].
Обнаружение
[править | править код]Для аналитического обнаружение остатки 2,4,5-трихлорфеноксиуксусной кислоты экстрагируют хлороформом и превращают путём очистки экстракта с помощью гидрохлорида пиридина в трихлорфенол. Образовавшийся трихлорфенол можно количественно выявить колориметрически по реакции с 4-аминоантипирином и феррицианидом калия. В качестве альтернативы очищенный экстракт 2,4,5-Т может быть этерифицирован с диметилсульфатом и определён с помощью газовой хроматографии[8].
Примечания
[править | править код]- ↑ 1 2 3 4 5 6 Record of 2,4,5-Trichlorphenoxyessigsäure in the GESTIS Substance Database of the IFA.
- ↑ 1 2 NIOSH Pocket Guide to Chemical Hazards #0583 (англ.). National Institute for Occupational Safety and Health (NIOSH).
- ↑ SUVA: Grenzwerte am Arbeitsplatz 2015 – MAK-Werte, BAT-Werte, Grenzwerte für physikalische Einwirkungen, abgerufen am 2. November 2015.
- ↑ 2,4,5-T. Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH). Дата обращения: 27 апреля 2017. Архивировано 8 июня 2017 года.
- ↑ 1 2 3 John Emsley. Dioxine, die tödlichsten Gifte der Welt? // Parfum, Portwein, PVC… (нем.). — Weinheim: Wiley-VCH, 2003. — ISBN 3-527-30789-3.
- ↑ Lenoir, D., H. Sandermann. Entstehung und Wirkung von Dioxinen (нем.) // Biologie in unserer Zeit. — 1993. — Bd. 23, Nr. 6. — S. 363—369. — ISSN 0045-205X.
- ↑ Generaldirektion Gesundheit und Lebensmittelsicherheit der Europäischen Kommission: Eintrag zu 2,4,5-T Архивная копия от 17 августа 2016 на Wayback Machine in der EU-Pestiziddatenbank; Eintrag in den nationalen Pflanzenschutzmittelverzeichnissen der Schweiz Архивная копия от 8 августа 2016 на Wayback Machine, Österreichs Архивная копия от 22 апреля 2016 на Wayback Machine und Deutschlands Архивная копия от 12 июля 2016 на Wayback Machine Архивная копия от 12 июля 2016 на Wayback Machine; abgerufen am 3.
- ↑ 1 2 Werner Perkow: Wirksubstanzen der Pflanzenschutz- und Schädlingsbekämpfungsmittel. 2. Auflage, Verlag Paul Parey.