Путь введения (Hrm, ffy;yunx)
Необходимо перенести содержимое этой статьи в статью Способ введения и заменить эту статью на перенаправление. |

В фармакологии и токсикологии путь введения представляет собой способ, с помощью которого лекарство, жидкость, токсин или другое вещество попадает в организм[1].
Пути введения веществ классифицируют по месту их применения. Наиболее распространенными являются пероральное и внутривенное введение. Пути введения также могут быть классифицированы в зависимости от локализации мишени действия. Действие может быть местным (локальным), энтеральным (системное действие с доставкой через желудочно-кишечный тракт) или парентеральным (системное действие с доставкой через другие пути, минуя желудочно-кишечный тракт). Путь введения и лекарственная форма являются аспектами, влияющими на доставку лекарств.
Классификация
[править | править код]Пути введения обычно классифицируются по месту применения (или экспозиции).
Путь активного вещества от места применения до места, где оно оказывает свое лечебное действие, обычно относится к области фармакокинетики (процессы введения, распределения и выведения лекарств). Исключение составляют трансдермальный и трансмукозальный пути введения, которые все ещё принято относить к путям введения.
Локализация целевого действия активных веществ обычно относится к области фармакодинамики (например, физиологический эффект лекарств [2]). Исключение составляет топическое применение, которое означает, что и место нанесения, и эффект имеют местный характер [3].
Иногда под местным применением понимают не только локальное место нанесения, но и локальный фармакодинамический эффект[3], а иногда только локальное место нанесения, независимо от места проявления эффекта[4][5].
По месту применения
Энтеральный/гастроинтестинальный (желудочно-кишечный) путь
Введение через желудочно-кишечный тракт иногда называют энтеральным или энтеральным введением (буквально означает «через кишечник»). Энтерально / энтеральное введение обычно включает пероральное[6] (через рот) и ректальное (в прямую кишку)[6] введение, которое характеризуется всасыванием через кишечник. Однако всасывание лекарств, принимаемых перорально, может происходить и в желудке, поэтому более подходящим термином для этого пути введения может быть гастроинтестинальный (через желудочно-кишечный тракт). Кроме того, некоторые места введения, часто классифицируемые как энтеральные, такие как сублингвальные[6] (под язык) и сублабиальные или трансбуккальные (между щекой и деснами/десной), всасываются в проксимальном отделе желудочно-кишечного тракта, не достигая кишечника. Строго энтеральное введение (непосредственно в кишечник) может использоваться для системного введения, а также местное (иногда называемое топическим), как, например, в контрастной клизме, когда контрастное вещество вводится в кишечник для визуализации. Однако для целей классификации, основанной на месте действия, термин «энтеральный» используется только для веществ, обладающих системным эффектом.

Многие лекарства в виде таблеток, капсул или капель принимаются перорально. Способы введения непосредственно в желудок включают введение через желудочный зонд или гастростомию. Вещества также могут вводиться в тонкий кишечник при помощи дуоденальной питательной трубки и энтерального питания. Таблетки с кишечнорастворимой оболочкой предназначены для растворения в кишечнике, а не в желудке, поскольку лекарство, содержащееся в таблетке, вызывает раздражение слизистой желудка.
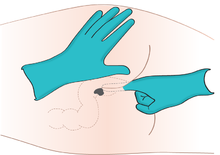
Ректальный путь является эффективным способом введения многих лекарств, особенно тех, которые используются в позднем возрасте[7][8][9][10][11][12][13]. Стенки прямой кишки быстро и эффективно впитывают большинство лекарств[14]. Лекарства, вводимые в дистальную треть прямой кишки, частично избегают эффекта первого прохождения через печень, что обеспечивает бо́льшую биодоступность многих лекарств по сравнению с пероральным путем. Слизистая оболочка прямой кишки представляет собой высоковаскуляризированную ткань, которая обеспечивает быстрое и эффективное всасывание лекарственных препаратов[15]. Суппозиторий — это твердая лекарственная форма, предназначенная для ректального введения. В хосписе специализированный ректальный катетер, предназначенный для удобного и незаметного введения текущих лекарств, обеспечивает практический способ доставки и удержания жидких препаратов в дистальном отделе прямой кишки, предоставляя медицинским работникам возможность пользоваться преимущества ректального введения. Один из примеров ректальной инфузии — инфузия с помощью капельницы Мерфи.
Парентеральный путь введения

Парентеральный (от др.-греч. παρά ‘мимо’ + ἔντερᾰ ‘кишечник’) путь включает любой путь, который не является энтеральным.
Парентеральное введение может осуществляться путем инъекции, то есть с помощью иглы (обычно подкожной) и шприца[16], или путем введения катетера.
Места применения парентерального введения следующие.
• Центральная нервная система:
- эпидурально, или перидурально (инъекция или инфузия в эпидуральное пространство), например эпидуральная анестезия;
- интрацеребрально (в головной мозг) — метод введения лекарства путем прямой инъекции в мозг; используется в экспериментальных исследованиях химических веществ[17] и лекарственных средств для лечения злокачественных опухолей мозга[18]. Интрацеребральный путь также может нарушить работу гематоэнцефалического барьера, не позволяя ему противостоять последующим инфекциям[19];
- интрацеребровентрикулярное (в мозговые желудочки) введение представляет собой введение в желудочковую систему мозга; применяется в последней линии опиоидной терапии для больных раком в терминальной стадии с трудноизлечимой раковой болью[20].
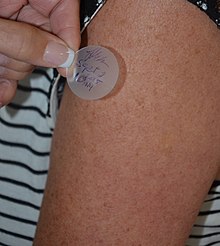

• Транскутанно (нанесение на кожу). Этот путь введения может использоваться как для местного воздействия (при проведении аллерготеста и типичной местной анестезии), так и для системного, характеризующееся проникновением активного вещества через кожу при трансдермальном применении.
• Сублингвальное и трансбуккальное введение лекарств — виды орального (через рот) пути введения лекарственного средства.
Сублингвальный прием лекарства осуществляется путем размещения лекарства под язык (лат. sub ‘под’ и lingua ‘язык’), где оно растворяется и всасывается в системный кровоток. Трансбуккальное введение предусматривает размещение препарата между десной и щекой (лат. trans ‘между’ и buccalis ‘щёчный’). Препараты для трансбуккального приема выпускаются в форме таблеток, пленок или спреев. Многие препараты предназначены для сублингвального приема, например сердечно-сосудистые средства, стероиды, барбитураты, опиоидные анальгетики с низкой биодоступностью в желудочно-кишечном тракте, ферменты, витамины и минералы.
• Экстраамниотическое введение осуществляется путем введения лекарства между эндометрием и плодными оболочками.
• Интраназальное введение (лат. intra ‘внутрь’ и nasus ‘нос’) используется для веществ местного действия, а также для инсуфляции, например для деконгестантных назальных спреев для всасывания через дыхательные пути. Такие вещества также называют ингаляционными, например ингаляционные анестетики.
• Внутриартериальные (в артерию), например сосудорасширяющие препараты для лечения ангиоспазма и тромболитические препараты для лечения эмболии.
• Внутрисуставное введение представляет собой инъекцию лекарства в сустав. В основном используется для облегчения симптомов при остеоартрите.
• Внутрисердечное введение (в сердце), например адреналин во время сердечно-легочной реанимации (больше не используется).
• Внутрикавернозная инъекция — введение препарата в основание полового члена.
• Внутрикожное введение (в саму кожу) используется для кожного теста на некоторые аллергены, а также для теста Манту на туберкулез.
• Интралезиональный путь введения (в очаг поражения кожи) используется при локальных поражениях кожи, например при лечении акне.
• Внутримышечное введение (в мышцу) применяется для введения многих вакцин, антибиотиков и психоактивных веществ длительного действия.
В рекреационных целях используется разговорный термин «наращивание мускула»[21].

• Внутриглазной путь введения применяется для введения лекарства в глаз, например некоторые препараты для лечения глаукомы или новообразований глаза.
• Внутрикостная инфузия (в костный мозг) направлена на непрямой внутривенный доступ, поскольку костный мозг впадает непосредственно в венозную систему. Данный путь введения лекарств и жидкостей используется в неотложной медицине и педиатрии в тех случаях, когда внутривенное введение затруднено.
• Внутрибрюшинное ведение, (инфузия или инъекция в брюшину), например перитонеальный диализ.
• Интратекально (в спинномозговой канал). Чаще всего используется для спинальной анестезии и химиотерапии.
• Внутриутробно.
• Внутривагинальное введение применяется для введения лекарственного вещества во влагалище.
• Внутривенно (в вену). Применяется для введения многих лекарств, например общее парентеральное питание.
• Внутрипузырная инфузия — в мочевой пузырь.
• Интравитреально (в глазное яблоко).
• Подкожно (под кожу)[22]. Обычно используется при подкожных инъекциях, например, инсулина. Помимо инъекций, возможно также медленное подкожное вливание жидкостей в виде гиподермоклизмы.
• Трансдермально (диффузия через неповрежденную кожу для системного, а не местного распределения), например трансдермальные терапевтические системы, такие как фентанил для обезболивания, никотиновые пластыри для лечения зависимости от курения и нитроглицерин для лечения стенокардии.
• Периваскулярное введение (периваскулярные медицинские устройства и периваскулярные системы доставки лекарств разработаны для локального применения вокруг кровеносного сосуда во время открытой сосудистой хирургии)[23].
• Трансмукозальные (диффузия через слизистую оболочку), например, инсуффляция (нюхание) кокаина, сублингвальные, то есть под язык, сублабиальные, то есть между губами и десной, нитроглицерин, вагинальные суппозитории.
Местный путь введения
Основная статья: Местная доставка лекарств
В определении местного способа применения иногда указывается, что и место нанесения, и фармакодинамический эффект являются местными[3].
В других случаях под местным применением понимается нанесение на участок тела независимо от места воздействия[4][5]. Согласно этому определению, местное применение также включает трансдермальное применение, при котором вещество помещается на кожу и всасывается в организм для достижения системного распределения.
Если определять топический путь применения строго как местное воздействие, то он может включать и энтеральное введение лекарств, которые плохо всасываются в желудочно-кишечном тракте. Одним из таких препаратов является антибиотик ванкомицин, который не всасывается в желудочно-кишечном тракте и используется только перорально для лечения псевдомембранозного колита[24].
Выбор пути введения
[править | править код]На выбор путей введения лекарств влияют различные факторы.
• Физические и химические свойства препарата.
• По физическим свойствам вещества классифицируются на твердые, жидкие и газообразные. Химические свойства включают растворимость, стабильность, рН, раздражающая способность и т. д.
• Место желаемого действия: действие может быть локальным и доступным или общим и недоступным.
• Скорость и степень всасывания препарата из различных путей.
• Влияние пищеварительных соков и эффект первого прохождения лекарств.
• Состояние здоровья пациента.
В экстренных ситуациях, при неотложной медицинской помощи и интенсивной терапии, лекарства чаще всего вводятся внутривенно. Это наиболее надежный путь, поскольку у тяжелобольных пациентов всасывание веществ из тканей и из пищеварительного тракта часто может быть непредсказуемым из-за изменения кровотока или моторики кишечника.
Удобство
Энтеральный путь введения, как правило, наиболее удобен для пациента, так как не требует проколов и стерильных условий. Поэтому при лечении хронических заболеваний предпочтение часто отдается препаратам, вводимым в организм энтеральным путем. Однако некоторые препараты нельзя применять энтерально, поскольку их всасывание в пищеварительном тракте незначительно или непредсказуемо. Трансдермальное введение является удобной альтернативой энтеральному пути введения, однако существует малое количество препаратов, которые для этого подходят.
Желаемый целевой эффект
Одинаковые препараты могут давать разные результаты в зависимости от пути введения. Например, некоторые препараты плохо всасываются в кровь из желудочно-кишечного тракта, поэтому их действие после энтерального введения отличается от действия после парентерального. Это можно проиллюстрировать на примере действия налоксона, антагониста опиатов, таких как морфин. Налоксон ингибирует действие опиатов в центральной нервной системе при внутривенном введении и поэтому используется при передозировке опиатами. Этот же препарат при проглатывании действует исключительно на кишечник. Данное свойство используется для лечения запоров при опиатной терапии и не влияет на обезболивающий эффект опиатов.
Пероральный путь введения
Пероральный путь, как правило, наиболее удобен и его использование обходится дешевле[25]. Однако некоторые препараты могут вызывать раздражение желудочно-кишечного тракта[26]. Для лекарств, выпускаемых в форме с замедленным высвобождением или с модифицированным высвобождением, разбивание таблеток или капсул может привести к более быстрой доставке лекарства, чем предполагалось[25]. Пероральный способ ограничен формами, содержащими только малые молекулы, в то время как биофармацевтические препараты (обычно белки) будут перевариваться в желудке и таким образом станут неэффективными. Биофармацевтические препараты должны вводиться инъекционно или в виде инфузий. Однако в ходе последних исследований были найдены различные способы повышения пероральной биодоступности этих препаратов. В частности, потенциал показали усилители проницаемости[27], ионные жидкости[28], наноносители на основе липидов[29], ингибиторы ферментов и микроиглы[30].
Пероральный прием часто обозначается PO — per os, что в переводе с латинского означает «через рот».
На биодоступность при пероральном приеме влияет количество препарата, которое всасывается через кишечный эпителий, и эффект первого прохождения[31].
Слизистая оболочка полости рта
Слизистая оболочка полости рта — это слизистая оболочка, выстилающая полость рта.
Трансбуккальный путь введения
При трансбуккальном введении лекарство помещается между деснами и внутренней поверхностью щеки[32][33]. По сравнению с подъязычной тканью ткань щеки менее проницаема, что приводит к более медленной абсорбции[33].
Сублабиальный путь введения
Основная статья: Сублабиальное введение
Сублингвальное введение
Сублингвальное введение осуществляется путем помещения препарата между языком и нижней поверхностью рта[33]. Слизистая оболочка подъязычной области обладает высокой проницаемостью, что обеспечивает доступ к лежащей под ней обширной сети капилляров, которые способствуют быстрому всасыванию лекарств[33].
Интраназальное введение
Введение лекарств через носовую полость обеспечивает их быстрое всасывание и быстрый терапевтический эффект[33]. Это связано с тем, что при всасывании лекарств через носовые ходы они не проходят через кишечник, прежде чем попасть в капилляры, а затем в системную циркуляцию, такой путь всасывания позволяет транспортировать лекарства в центральную нервную систему по путям обонятельного и тройничного нервов[33].
Вещества, для которых характерна интраназальная абсорбция, в основном обладают низкой липофильностью и большим размером молекул. При интраназальном пути введения важную роль в снижении биодоступности лекарственных препаратов играет их ферментативная деградация в носовой полости и мукоцилиарный клиренс со слизистой оболочки[33].

Местное применение
Благодаря доставке лекарств практически непосредственно к месту действия снижается риск возникновения системных побочных эффектов[25].
Абсорбция на коже (дермальная абсорбция), например, заключается в прямой доставке лекарства в кожу и затем в системную циркуляцию[34]. Однако может возникнуть раздражение кожи, так как для некоторых лекарственных форм, таких как кремы или лосьоны, трудно контролировать дозировку[26]. При контакте с кожей препарат проникает в омертвевший роговой слой, а затем может достичь живого эпидермиса, дермы и кровеносных сосудов[34].
Парентеральное введение
Парентеральный (от др.-греч. παρά ‘мимо’ + ἔντερᾰ ‘кишечник’) путь включает любой путь, который не является энтеральным. Этот термин в основном используется для обозначения четырёх наиболее известных способов введения.


Термин «инъекция» включает внутривенное (В/В), внутримышечное (В/М), подкожное (П/К) и внутрикожное (В/К) введение[35].
Парентеральное введение обычно действует быстрее, чем местное или энтеральное: начало действия часто наступает через 15-30 секунд при внутривенном введении, через 10-20 минут при внутримышечном и через 15-30 минут при подкожном введении[36]. Кроме того, данные пути введения обладают практически 100%-й биодоступностью и могут использоваться для препаратов, которые плохо всасываются или неэффективны при пероральном приеме[25]. Например, некоторые антипсихотики можно вводить в виде внутримышечных инъекций длительного действия[37]: этот способ часто используется с применением физической силы в присутствии представителей правоохранительных органов и против воли пациента. Однако все дозы инъекций антипсихотиков длительного действия сопряжены с огромным риском для здоровья и самочувствия пациента. Таким образом, следует учитывать исключительные этические соображения. Если выбор сделан в пользу применения силы, то следует использовать только наименьшую дозу, которая в настоящее время научно доказана как эффективная для конкретного препарата. Это связано с тем, что, несмотря на инъекционное введение, препараты имеют тяжелые этерифицирующие молекулярные соединения, благодаря которым следы наркотика могут находиться в организме до одного года.
Непрерывные внутривенные инфузии могут использоваться для непрерывного введения лекарств или жидкостей[38].
К недостаткам инъекций относятся боль или дискомфорт для пациента при введении, а также необходимость наличия квалифицированного персонала, использующего методы асептики для введения препарата[25]. Однако в некоторых случаях пациентов учат самостоятельно делать инъекции, например пациенты с инсулинозависимым сахарным диабетом самостоятельно проводят подкожное введение инсулина. Поскольку при внутривенном введении препарат доставляется к месту действия очень быстро, существует риск передозировки и повышается риск побочных эффектов[25].
Дыхательные пути
Ингаляция через рот


Ингаляционные препараты быстро всасываются и действуют как местно, так и системно[26]. Для получения правильной дозы необходима правильная техника использования ингаляторов. Некоторые лекарства могут иметь неприятный вкус или раздражать полость рта[26]. Как правило, при вдыхании через рот в легкие попадает только 20-50 % дозы, содержащейся в порошкообразных частицах[47]. Оставшиеся 50-70 % неосажденных аэрозольных частиц выводятся из легких при выдохе[47].
Вдыхаемые порошкообразные частицы размером >8 мкм предрасположены к осаждению в центральных и проводящих дыхательных путях (проводящая зона) за счет инерционного уплотнения[47].
Вдыхаемые порошкообразные частицы диаметром от 3 до 8 мкм в основном оседают в переходных зонах легких путем седиментации[47].
Вдыхаемые порошкообразные частицы диаметром <3 мкм структурно предрасположены к осаждению преимущественно в респираторных отделах легких посредством диффузии[47].
Частицы, оседающие в верхних и центральных дыхательных путях, обычно в значительной степени абсорбируются системно, поскольку они лишь частично удаляются мукоцилиарным клиренсом, что приводит к пероральному всасыванию при проглатывании транспортированной слизи, а эффект первого прохождения или неполное всасывание в результате потери с калом могут иногда снижать биодоступность[48]. Это ни в коем случае не должно наводить клиницистов или исследователей на мысль, что вдыхаемые частицы не представляют большей опасности, чем проглатываемые. Это лишь означает, что сочетание обоих методов может иметь место независимо от размера или липо-гидрофильности различных поверхностей частиц[47].
Дополнительная информация: PM 2.5 и PM 10.
Назальная ингаляция
Ингаляция вещества через нос практически идентична пероральной ингаляции, за исключением того, что часть препарата всасывается интраназально, а не в ротовой полости, прежде чем попасть в дыхательные пути. Оба метода характеризуются различным количеством вещества, откладываемого в соответствующих начальных полостях, и уровень слизи в любой из этих полостей будет отражать количество поступившего вещества. Скорость вдыхания влияет на количество вещества, которое попадет в легкие. Быстрое вдыхание приводит к более быстрому усвоению, поскольку большее количество вещества попадает в легкие. Вещества в форме, которая препятствует всасыванию в легких, вероятно, будут сопротивляться всасыванию в носовом проходе и полости рта и часто становятся ещё более устойчивыми к всасыванию после того, как они не всосутся в первых полостях и проглатываются.
Исследование
[править | править код]Доставка лекарств по нервам является следующим шагом после обычного добавления факторов роста в нервные проводящие каналы. Системы доставки лекарств позволяют регулировать скорость высвобождения факторов роста во времени, что позволяет создать условия, наиболее близкие к условиям разработки in vivo[49].
См. также
[править | править код]- ADME
- Катетер
- Лекарственная форма
- Инъекция лекарства
- Инстилляция в ухо
- Медицинские иглы
- Синдром внутривенной марихуаны
- Список медицинских ингаляторов
- Наномедицина
- Абсорбция (фармакология)
Примечания
[править | править код]- ↑ Route of administration (англ.). TheFreeDictionary.com. Дата обращения: 6 июня 2024. Архивировано 4 июля 2023 года.
- ↑ D. N. LeVine, L. Kidd, O. A. Garden, M. B. Brooks, R. Goggs, B. Kohn, A. J. Mackin, E. R. B. Eldermire, Y. M. Chang, J. Allen, P. W. Christopherson, B. Glanemann, H. Maruyama, M. C. Naskou, L. N. Nielsen, S. Shropshire, A. K. Viall, A. J. Birkenheuer, M. A. Forman, A. S. Hanzlicek, K. F. Langner, E. Lashnits, K. F. Lunn, K. M. Makielski, X. Roura, E. Spada. ACVIM consensus statement on the diagnosis of immune thrombocytopenia in dogs and cats (англ.). — 2024-05-16. — ISSN 0891-6640. — doi:10.1111/jvim.16996. Архивировано 20 июня 2024 года.
- ↑ 1 2 3 Route of administration
- ↑ 1 2 topical // The Free Dictionary. Архивировано 6 июня 2024 года.
- ↑ 1 2 Dictionary.com | Meanings & Definitions of English Words (англ.). Dictionary.com. Дата обращения: 6 июня 2024.
- ↑ 1 2 3 "Oklahoma Administrative Code and Register > 195:20-1-3.1. Pediatric conscious sedation utilizing enteral methods (oral, rectal, sublingual)". Дата обращения: 20 июня 2024. Архивировано из оригинала 22 июля 2011 года.
- ↑ Mellar P. Davis, Declan Walsh, Susan B. LeGrand, Michael Naughton. Symptom control in cancer patients: the clinical pharmacology and therapeutic role of suppositories and rectal suspensions (англ.) // Supportive Care in Cancer. — 2002-03-01. — Vol. 10, iss. 2. — P. 117–138. — ISSN 1433-7339. — doi:10.1007/s00520-001-0311-6.
- ↑ A. G. de Boer, F. Moolenaar, L. G. J. de Leede, D. D. Breimer. Rectal Drug Administration (англ.) // Clinical Pharmacokinetics. — 1982-08-01. — Vol. 7, iss. 4. — P. 285–311. — ISSN 1179-1926. — doi:10.2165/00003088-198207040-00002.
- ↑ Ewoud J. van Hoogdalem, Albertus G. de Boer, Douwe D. Breimer. Pharmacokinetics of Rectal Drug Administration, Part I (англ.) // Clinical Pharmacokinetics. — 1991-07-01. — Vol. 21, iss. 1. — P. 11–26. — ISSN 1179-1926. — doi:10.2165/00003088-199121010-00002.
- ↑ Ewoud J. van Hoogdalem, Albertus G. de Boer, Douwe D. Breimer. Pharmacokinetics of Rectal Drug Administration, Part II (англ.) // Clinical Pharmacokinetics. — 1991-08-01. — Vol. 21, iss. 2. — P. 110–128. — ISSN 1179-1926. — doi:10.2165/00003088-199121020-00003.
- ↑ F Moolenaar. Biopharmaceutics of rectal administration of drugs in man 7. Absorption rate and bioavailability of phenobarbital and its sodium salt from rectal dosage forms // International Journal of Pharmaceutics. — 1979-12. — Т. 4, вып. 2. — С. 99–109. — ISSN 0378-5173. — doi:10.1016/0378-5173(79)90057-7.
- ↑ Nina M. Graves, Gregory B. Holmes, Robert L. Kriel, Carolyn Jones-Saete, Betty Ong, David J. Ehresman. Relative Bioavailability of Rectally Administered Phenobarbital Sodium Parenteral Solution (англ.) // DICP. — 1989-07. — Vol. 23, iss. 7—8. — P. 565–568. — ISSN 1042-9611. — doi:10.1177/1060028089023007-806. Архивировано 10 октября 2023 года.
- ↑ F. Moolenaar, S. Bakker, J. Visser, T. Huizinga. Biopharmaceutics of rectal administration of drugs in man IX. Comparative biopharmaceutics of diazepam after single rectal, oral, intramuscular and intravenous administration in man // International Journal of Pharmaceutics. — 1980-04. — Т. 5, вып. 2. — С. 127–137. — ISSN 0378-5173. — doi:10.1016/0378-5173(80)90017-4.
- ↑ HPNA.org. web.archive.org (26 января 2013). Дата обращения: 6 июня 2024. Архивировано 26 января 2013 года.
- ↑ # 257 Use of Rectal Meds for Palliative Care Patients. web.archive.org (2 июня 2014). Дата обращения: 6 июня 2024. Архивировано из оригинала 2 июня 2014 года.
- ↑ injection Meaning in the Cambridge English Dictionary. web.archive.org (30 июля 2017). Дата обращения: 6 июня 2024. Архивировано 30 июля 2017 года.
- ↑ MDMA (Ecstasy) Metabolites and Neurotoxicity -- Neurotransmitter.net. www.neurotransmitter.net. Дата обращения: 6 июня 2024. Архивировано 30 ноября 2023 года.
- ↑ R. O. McKeran, G. Firth, S. Oliver, D. Uttley, S. O'Laoire. A potential application for the intracerebral injection of drugs entrapped within liposomes in the treatment of human cerebral gliomas. (англ.) // Journal of Neurology, Neurosurgery & Psychiatry. — 1985-12-01. — Vol. 48, iss. 12. — P. 1213–1219. — ISSN 0022-3050. — doi:10.1136/jnnp.48.12.1213. Архивировано 6 июня 2024 года.
- ↑ James L. Wright, Randall E. Merchant. Blood-brain barrier changes following intracerebral injection of human recombinant tumor necrosis factor-α in the rat (англ.) // Journal of Neuro-Oncology. — 1994-02-01. — Vol. 20, iss. 1. — P. 17–25. — ISSN 1573-7373. — doi:10.1007/BF01057957.
- ↑ Leonidas C. Goudas, Agnes Langlade, Alain Serrie, Wayne Matson, Paul Milbury, Claude Thurel, Pierre Sandouk, Daniel B. Carr. Acute Decreases in Cerebrospinal Fluid Glutathione Levels after Intracerebroventricular Morphine for Cancer Pain (англ.) // Anesthesia & Analgesia. — 1999-11. — Т. 89, вып. 5. — С. 1209. — ISSN 0003-2999. — doi:10.1213/00000539-199911000-00023. Архивировано 6 июня 2024 года.
- ↑ Fenway Community Health: Crystal Meth The Effects. web.archive.org (10 декабря 2010). Дата обращения: 6 июня 2024. Архивировано из оригинала 10 декабря 2010 года.
- ↑ Eric J. Nestler, Steven E. Hyman, Robert C. Malenka. Molecular neuropharmacology: a foundation for clinical neuroscience. — 2. ed., [Nachdr.]. — New York, NY: McGraw-Hill Medical, 2010. — 498 с. — ISBN 978-0-07-148127-4.
- ↑ Ioanna Mylonaki, Éric Allémann, François Saucy, Jacques-Antoine Haefliger, Florence Delie, Olivier Jordan. Perivascular medical devices and drug delivery systems: Making the right choices // Biomaterials. — 2017-06. — Т. 128. — С. 56–68. — ISSN 0142-9612. — doi:10.1016/j.biomaterials.2017.02.028.
- ↑ Vancomycin Monograph for Professionals (англ.). Drugs.com. Дата обращения: 6 июня 2024. Архивировано 6 июня 2024 года.
- ↑ 1 2 3 4 5 6 Contributor, N. T. The administration of medicines (англ.). Nursing Times (19 ноября 2007). Дата обращения: 6 июня 2024. Архивировано 2 января 2020 года.
- ↑ 1 2 3 4 DDS (англ.). CT.gov. Дата обращения: 6 июня 2024. Архивировано 6 июня 2024 года.
- ↑ Akira Yamamoto, Hiroki Ukai, Masaki Morishita, Hidemasa Katsumi. Approaches to improve intestinal and transmucosal absorption of peptide and protein drugs // Pharmacology & Therapeutics. — 2020-07-01. — Т. 211. — С. 107537. — ISSN 0163-7258. — doi:10.1016/j.pharmthera.2020.107537.
- ↑ Amrita Banerjee, Kelly Ibsen, Tyler Brown, Renwei Chen, Christian Agatemor, Samir Mitragotri. Ionic liquids for oral insulin delivery (англ.) // Proceedings of the National Academy of Sciences. — 2018-07-10. — Vol. 115, iss. 28. — P. 7296–7301. — ISSN 0027-8424. — doi:10.1073/pnas.1722338115. Архивировано 6 июня 2024 года.
- ↑ Soheil Haddadzadegan, Farid Dorkoosh, Andreas Bernkop-Schnürch. Oral delivery of therapeutic peptides and proteins: Technology landscape of lipid-based nanocarriers // Advanced Drug Delivery Reviews. — 2022-03-01. — Т. 182. — С. 114097. — ISSN 0169-409X. — doi:10.1016/j.addr.2021.114097. Архивировано 6 июня 2024 года.
- ↑ Sam Maher, David J. Brayden. Formulation strategies to improve the efficacy of intestinal permeation enhancers, // Advanced Drug Delivery Reviews. — 2021-10-01. — Т. 177. — С. 113925. — ISSN 0169-409X. — doi:10.1016/j.addr.2021.113925. Архивировано 6 июня 2024 года.
- ↑ Mary F. Hebert. 3 - Impact of Pregnancy on Maternal Pharmacokinetics of Medications // Clinical Pharmacology During Pregnancy / Donald R. Mattison. — Academic Press, 2013-01-01. — С. 17–39. — ISBN 978-0-12-386007-1. — doi:10.1016/b978-0-12-386007-1.00003-9. Архивировано 13 февраля 2023 года.
- ↑ Drug Absorption - Clinical Pharmacology (англ.). MSD Manual Professional Edition. Дата обращения: 6 июня 2024. Архивировано 31 октября 2019 года.
- ↑ 1 2 3 4 5 6 7 Bonnie M. Kaminsky, Jolene R. Bostwick, Sally K. Guthrie. Alternate Routes of Administration of Antidepressant and Antipsychotic Medications (англ.) // Annals of Pharmacotherapy. — 2015-07. — Vol. 49, iss. 7. — P. 808–817. — ISSN 1060-0280. — doi:10.1177/1060028015583893. Архивировано 10 октября 2023 года.
- ↑ 1 2 Francisca Rodrigues, Maria Beatriz P. P. Oliveira. 3.8 - Cell-based in vitro models for dermal permeability studies // Concepts and Models for Drug Permeability Studies / Bruno Sarmento. — Woodhead Publishing, 2016-01-01. — С. 155–167. — ISBN 978-0-08-100094-6. — doi:10.1016/b978-0-08-100094-6.00010-9. Архивировано 13 февраля 2023 года.
- ↑ List of Error-Prone Abbreviations (англ.). ECRI and ISMP. Дата обращения: 6 июня 2024. Архивировано 6 июня 2024 года.
- ↑ Routes for Drug Administration (англ.) // Emergency Treatment Guidelines Appendix. Manitoba Health.. — 2003. — August. Архивировано 1 октября 2013 года.
- ↑ Stahl SM. Stahl's Essential Psychopharmacology: Neuroscientific basis and practical applications (англ.) // New York: Cambridge University Press. — 2008.
- ↑ Smeltzer SC Bare BG. Textbook of Medical-Surgical Nursing // 9th ed, Lippincott. — 2000.
- ↑ Ali, Mohammed. Pulmonary Drug Delivery // Handbook of Non-Invasive Drug Delivery Systems. — Elsevier, 2010. — P. 209–246. — ISBN 978-0-8155-2025-2. — doi:10.1016/b978-0-8155-2025-2.10009-5.
- ↑ Lungs - Anatomy of the Respiratory System. archive.is (29 марта 2020). Дата обращения: 29 марта 2020. Архивировано из оригинала 29 марта 2020 года.
- ↑ Major Zones & Divisions. GetBodySmart (30 октября 2017). Дата обращения: 29 марта 2020.
- ↑ Diagram for conducting zone. Дата обращения: 29 марта 2020. Архивировано 29 марта 2020 года.
- ↑ Diagram for respiratory zone. Дата обращения: 29 марта 2020. Архивировано 29 марта 2020 года.
- ↑ Diagram for upper respiratory tract. Дата обращения: 29 марта 2020. Архивировано 29 марта 2020 года.
- ↑ Diagram for lower respiratory tract. Дата обращения: 29 марта 2020. Архивировано 29 марта 2020 года.
- ↑ Diagram for majour zones of respiratory system. Дата обращения: 29 марта 2020. Архивировано 29 марта 2020 года.
- ↑ 1 2 3 4 5 6 Hemal Tandel, Kiruba Florence, Ambikanandan Misra. Protein and Peptide Delivery through Respiratory Pathway // Challenges in Delivery of Therapeutic Genomics and Proteomics. — Elsevier, 2011. — С. 429–479. — ISBN 978-0-12-384964-9. — doi:10.1016/b978-0-12-384964-9.00009-8.
- ↑ Ximena M. Bustamante-Marin, Lawrence E. Ostrowski. Cilia and Mucociliary Clearance (англ.) // Cold Spring Harbor Perspectives in Biology. — 2017-04-01. — Vol. 9, iss. 4. — P. a028241. — ISSN 1943-0264. — doi:10.1101/cshperspect.a028241. Архивировано 17 июня 2024 года.
- ↑ E. Lavik, R. Langer. Tissue engineering: current state and perspectives // Applied Microbiology and Biotechnology. — 2004-07. — Т. 65, вып. 1. — С. 1–8. — ISSN 0175-7598. — doi:10.1007/s00253-004-1580-z. Архивировано 6 июня 2024 года.
Ссылки
[править | править код]- The 10th US-Japan Symposium on Drug Delivery Systems
- FDA Center for Drug Evaluation and Research Data Standards Manual: Route of Administration
- FDA Center for Drug Evaluation and Research Data Standards Manual: Dosage Form
- A.S.P.E.N. American Society for Parenteral and Enteral Nutrition
- As Drug+Administration+Routes в Национальной медицинской библиотеке медицинских предметных рубрик (МПР)
На эту статью не ссылаются другие статьи Википедии. |