Презентация антигена (Hjy[yumgenx gumniyug)

Презентация антиге́на (англ. antigen presentation) — процесс предъявления T-лимфоциту фрагмента антигена с целью запуска T-клеточного ответа. Поскольку T-клетки не распознают нативные антигены, то нативные антигены предварительно фрагментируются антигенпрезентирующей клеткой, и фрагменты выставляются на её поверхности в связанном с главным комплексом гистосовместимости (MHC) виде, чтобы они могли быть распознаны T-клеточными рецепторами. В случае вирусной или бактериальной инфекции антигенпрезентирующая клетка выставляет на своей поверхности эндогенные или экзогенные пептидные фрагменты, полученные от исходного антигена, в виде комплекса с MHC. Существуют два класса молекул MHC, которые различаются происхождением фрагментов антигена, которые с ними связываются: молекулы MHC I класса[англ.] (MHC-I) связывают пептидные фрагменты, происходящие из цитозоля клетки (то есть эндогенные), а молекулы MHC II класса[англ.] (MHC-II) связывают фрагменты экзогенного происхождения, которые появились в результате эндоцитоза исходного антигена и его последующего расщепления[1]. Каждая T-клетка способна распознавать от нескольких десятков до нескольких сотен фрагментов одного и того же антигена, хотя на поверхности антигенпрезентирующей клетки могут быть экспонированы тысячи других пептидных фрагментов, поскольку одна и та же молекула MHC способна связывать самые разнообразные пептиды[2][3].
В отличие от Т-клеток, B-клетки способны с помощью B-клеточных рецепторов связывать интактные антигены с их нативной структурой, а не их линейные пептидные фрагменты.
Презентация внутриклеточных антигенов
[править | править код]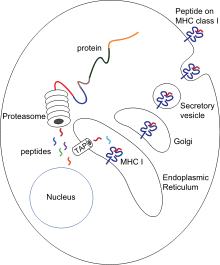
Цитотоксические T-клетки, также известные как T-киллеры, отличаются экспрессией корецептора CD8 и специализируются на том, что вызывают программируемую клеточную гибель других клеток. Когда T-киллеры обнаруживают признаки болезни — вирусной инфекции, инфекции, вызванной внутриклеточными бактериями, или злокачественные клетки — они запускают гибель потенциально опасных клеток (то есть клеток, заражённых вирусом или внутриклеточными бактериями, а также злокачественных клеток). Все клетки, имеющие ядра, а также тромбоциты экспрессируют MHC I класса, молекулы которого располагаются в клеточной мембране. Антигены, подвергшиеся процессингу в этих клетках, выставляются на их поверхности в комплексе с молекулами MHC I класса[4][5].
В ходе процессинга антигена исходный антиген расщепляется на короткие пептиды цитозольными протеазами. Далее полученные пептидные фрагменты доставляются в эндоплазматический ретикулум (ЭПР) при участии белков теплового шока и транспортёром, связанным с процессингом антигена[англ.] (англ. transporter associated with antigen processing, TAP). TAP переносит цитозольные пептиды в люмен ЭПР с затратой АТФ. В люмене ЭПР имеется несколько шаперонов, связанных со сборкой MHC-I, а именно, кальнексин[англ.], кальретикулин[англ.] и тапазин[англ.]. Пептиды загружаются на MHC-I через пептид-связывающую бороздку, которая расположена между двумя α-спиралями в нижней части доменов α1 и α2 MHC-I. Когда от комплекса MHC-I с фрагментом антигена (pMHC-I) отделяется тапазин, pMHC-I выходит из ЭПР и транспортируется к поверхности клетки внутри экзоцитозных везикул[6].
Наивные[англ.] CD8+ T-клетки не могут непосредственно убить инфицированную или злокачественную клетку. Они должны быть активированы комплексом pMHC-I, который несёт антигенпрезентирующая клетка. Антиген может быть презентирован непосредственно по механизму, описанному выше, или с помощью кросс-презентации[англ.] от инфицированных или неинфицированных клеток. После взаимодействия pMHC-I с T-клеточным рецептором на поверхности наивной CD8+ T-клетки при участии костимулирующих сигналов и/или цитокинов T-клетка активируется и мигрирует в периферические ткани, где убивает клетки, экспрессирующие тот антиген, которые ей был представлен[7].
В ходе кросс-презентации молекулы MHC-I презентируют внеклеточные антигены, которые обычно презентируются MHC-II. Такой способностью обладают MHC-I некоторых антигенпрезентирующих клеток, в особенности, плазмацитоидные дендритные клетки[англ.]. Кросс-презентация происходит тогда, когда антигенпрезентирующая клетка не инфицирована сама, но запускает локальный противовирусный или противоопухолевый иммунный ответ без миграции в близлежащие лимфоузлы[5].
Презентация внеклеточных антигенов
[править | править код]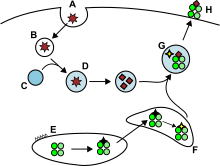
Антигены из внеклеточного пространства, а также некоторые эндогенные антигены заключаются в эндоцитозные везикулы, доставляются на поверхность клетки и связываются молекулами MHC-II. Их распознают T-хелперы, экспрессирующие корецептор CD4. Только дендритные клетки, B-клетки и макрофаги экспрессируют MHC-II в достаточном количестве, поэтому экспрессия MHC-II более специфична, чем экспрессия MHC-I[8].
Антигенпрезентирующие клетки, как правило, поглощают антиген из внеклеточного пространства с помощью эндоцитоза, а также пиноцитоза, макроаутофагии, эндосомной микроаутофагии или аутофагии, опосредованной шаперонами[англ.]. В случае эндоцитоза антигены попадают в везикулы, называемые эндосомами. В процессинге антигена задействованы три компартмента: ранние эндосомы, поздние эндосомы, или эндолизосомы, и лизосомы, в которых антигены гидролизуются лизосомными ферментами (кислыми гидролазами[англ.], глюкозидазами[англ.], протеазами, липазами). Расщеплению способствует постепенное понижение pH в везикулах. Главную роль в расщеплении антигена играют эндосомные гидролазы катепсины, разрезающие антиген на короткие пептиды[8].
Молекулы MHC-II транспортируются из ЭПР в погрузочный компартмент для MHC-II в месте с полипептидом, известным как инвариантная цепь (Ii, CD74). Специфическая молекула класса MHC-II (HLA-DO[англ.] и HLA-DM[англ.]) катализируют обмен части CD74, известный как CLIP-пептид[англ.], на фрагмент антигена. Образовавшийся комплекс пептид-MHC-II (pMHC-II) транспортируется в клеточную мембрану, где фрагмент антигена презентируется T-хелперам в лимфоузлах[6].
Мигрируя к лимфоидным тканям с помощью хемотаксических сигналов, антигенпрезентирующие клетки проходят процесс созревания, в ходе которого они утрачивают способность к фагоцитозу и становятся более способными к взаимодействию с T-клетками и презентации им антигена. Как и в случае T-киллеров, для активации T-хелперов, помимо pMHC-II, необходимы дополнительные костимулирующие сигналы[9].
Презентация нативных антигенов B-клеткам
[править | править код]B-клеточные рецепторы, располагающиеся на поверхности B-клеток, связываются с нерасщеплёнными антигенами, имеющими нативную конформацию, а не с линейными пептидными фрагментами антигенов в комплексе с MHC. Большие комплексы интактных антигенов презентируются B-клеткам в лимфоузлах фолликулярными дендритными клетками в форме иммунных комплексов[англ.]. Некоторые антигенпрезентирующие клетки экспрессируют сниженное количество лизосомных ферментов, благодаря чему могут презентировать B-клеткам нерасщеплённые антигены[10][11].
Примечания
[править | править код]- ↑ Charles A Janeway, Jr; Travers, Paul; Walport, Mark; Shlomchik, Mark J. Antigen Presentation to T Lymphocytes (англ.) : journal. — 2001. — 1 January. Архивировано 15 сентября 2019 года.
- ↑ Purcell A. W., Croft N. P., Tscharke D. C. Immunology by numbers: quantitation of antigen presentation completes the quantitative milieu of systems immunology! (англ.) // Current Opinion In Immunology. — 2016. — June (vol. 40). — P. 88—95. — doi:10.1016/j.coi.2016.03.007. — PMID 27060633.
- ↑ Charles A Janeway, Jr; Travers, Paul; Walport, Mark; Shlomchik, Mark J. The major histocompatibility complex and its functions (англ.) : journal. — 2001. — 1 January. Архивировано 27 апреля 2016 года.
- ↑ Hewitt E. W. The MHC class I antigen presentation pathway: strategies for viral immune evasion. (англ.) // Immunology. — 2003. — October (vol. 110, no. 2). — P. 163—169. — doi:10.1046/j.1365-2567.2003.01738.x. — PMID 14511229.
- ↑ 1 2 Joffre O. P., Segura E., Savina A., Amigorena S. Cross-presentation by dendritic cells. (англ.) // Nature Reviews. Immunology. — 2012. — 13 July (vol. 12, no. 8). — P. 557—569. — doi:10.1038/nri3254. — PMID 22790179.
- ↑ 1 2 Bhattacharya, J. K. Sinha & S. A Text Book of Immunology (англ.). — Academic Publishers. — ISBN 9788189781095.
- ↑ Sei J. J., Haskett S., Kaminsky L. W., Lin E., Truckenmiller M. E., Bellone C. J., Buller R. M., Norbury C. C. Peptide-MHC-I from Endogenous Antigen Outnumber Those from Exogenous Antigen, Irrespective of APC Phenotype or Activation. (англ.) // PLoS Pathogens. — 2015. — June (vol. 11, no. 6). — P. e1004941—1004941. — doi:10.1371/journal.ppat.1004941. — PMID 26107264.
- ↑ 1 2 Stern L. J., Santambrogio L. The melting pot of the MHC II peptidome. (англ.) // Current Opinion In Immunology. — 2016. — June (vol. 40). — P. 70—77. — doi:10.1016/j.coi.2016.03.004. — PMID 27018930.
- ↑ Flores-Romo L. In vivo maturation and migration of dendritic cells. (англ.) // Immunology. — 2001. — March (vol. 102, no. 3). — P. 255—262. — doi:10.1046/j.1365-2567.2001.01204.x. — PMID 11298823.
- ↑ Batista F. D., Harwood N. E. The who, how and where of antigen presentation to B cells. (англ.) // Nature Reviews. Immunology. — 2009. — January (vol. 9, no. 1). — P. 15—27. — doi:10.1038/nri2454. — PMID 19079135.
- ↑ Harwood N. E., Batista F. D. Antigen presentation to B cells. (англ.) // F1000 Biology Reports. — 2010. — 17 December (vol. 2). — P. 87—87. — doi:10.3410/B2-87. — PMID 21283653.
Эта статья входит в число добротных статей русскоязычного раздела Википедии. |