Алахлор (Glg]lkj)
| Алахлор | |
|---|---|
   | |
| Общие | |
| Систематическое наименование |
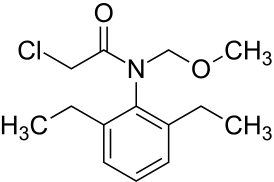
2-Хлор-N-(2,6-диэтилфенил)-N-(метоксиметилфенил)ацетамид |
| Хим. формула | C14H20ClNO2 |
| Физические свойства | |
| Состояние | От бесцветного до серого цвета, слабо душистый, легковоспламеняющийся порошок |
| Молярная масса | 269,767 г/моль |
| Плотность | 1,12 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 40–41 °C |
| • кипения | 100 °C (при 3 Па)[1] °C |
| • разложения | 105 °C[2] |
| Химические свойства | |
| Растворимость | |
| • в воде | плохо растворим (212 мг·л−1 при 20 °C)[1] |
| Классификация | |
| Рег. номер CAS | 15972-60-8 |
| PubChem | 2078 |
| Рег. номер EINECS | 240-110-8 |
| SMILES | |
| InChI | |
| ChEBI | 2533 |
| ChemSpider | 1994 |
| Безопасность | |
| ЛД50 |
930 мг·кг−1 (крыса, орально)[1]
|
| Фразы риска (R) | R22 R40 R43 R50/53 |
| Фразы безопасности (S) | (S2) S36/37 S46 S60 S61 |
| Краткие характер. опасности (H) |
H302, H317, H351, H410 |
| Меры предостор. (P) |
P273, PP280, 501 |
| Пиктограммы СГС |
|
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Алахлор — гербицид из группы хлорацетанилидов. Это белое твёрдое вещество без запаха. Широко применяется для контроля однолетних трав и широколиственных сорняков на посевах культурных растений. Использования алахлора в качестве гербицида запрещено в Европейском Союзе[3].
Механизм действия основан на ингибирования элонгазы и геранилгеранилпирофосфат циклизующих ферментов, ключевых энзимов пути синтеза гиббереллинов[4].
Алахлор был зарегистрирован компанией Monsanto в 1969 году и появился на рынке США под торговым названием Lasso[5].
Синтез
[править | править код]Алахлор получают путем последовательной реакции 2,6-диметиланилина с формальдегидом, хлорацетилхлоридом и метанольным раствором аммиака.
Использование
[править | править код]Алахлор применяется для уничтожения однолетних и широколиственных сорняков на посевах капусты, кукурузы, арахиса, сои, хлопка, рапса и подсолнечника[6]. Является вторым наиболее широко используемым гербицидом в США, где особо широко применяется на плантациях кукурузы и сои[7].
Детали применения
[править | править код]Алахлор хорошо смешивается с другими гербицидами. Он продается в виде смеси с атразином, глифосатом, трифлуралином и имазахином. Это селективный, системный гербицид, который хорошо поглощается прорастающими всходами и корнями. Нарушая синтез растительных гормонов гиббириллинов, он вызывает нарушение синтеза белка остановку роста корней[8][9].
Обычно выпускается в виде микрогранул, содержащих 15 % активного ингредиента или в виде эмульгируемого концентрата, с концентрацией алахлора 480 г/л. Препарат либо помещают в лунки перед посадкой, либо опрыскивают почву до появления всходов[10].
Токсикология
[править | править код]Алахлор малотоксичен, но классифицируется как потенциально канцерогенное вещество[2]. Он особенно токсичен для водорослей, мелких ракообразных и рыб[11]. Может проникать в грунтовые воды с осадками и накапливаться в плодах и семенах. По этой причине в ЕС существуют специальные нормы, регулирующие его содержание в продуктах питания.
Воздействия на окружающую среду
[править | править код]Алахлор умеренной сорбируется почвой. Незначительная часть препарада распадается под воздействием света. Деградация в почве в значительной степени биологически опосредованна, и заканчивается образованием несколько метаболитов. Период полураспада в почве в аэробных условиях колеблется от 6 до 15 дней и значительно снижается в анаэробных условиях[12]. Одно из возможных объяснений для такого эффекта основано на наблюдении, что в безкислородной среде алахлор стремительно превращается в порядко 14 продуктов деградации в присутствии железистых смектитов. Железо в таких минералах может быть использовано некоторыми почвенными бактериями в качестве акцептора электронов, когда почва затоплена, поэтому процесс трансформации гербицида значительно ускоряется за счёт микробиологического распада[13]. Аналогичные наблюдения существуют для гербицидов трифлуралина и атразина.
Алахлор часто используется в школьных кабинетах химии в качестве реагента для демонстраций, таких как горение магния. Алахлор может быть использован в качестве замены для метана в таком эксперименте, когда газ недоступен[14].
См. также
[править | править код]Примечания
[править | править код]- ↑ 1 2 3 4 Record of Alachlor in the GESTIS Substance Database of the IFA.
- ↑ 1 2 WHO/FAO Data Sheet on Pesticides (PDS) für Alachlor Архивная копия от 28 октября 2016 на Wayback Machine, abgerufen am 9. Dezember 2014.
- ↑ Thomas D. Boyer; Michael Peter Manns; Arun J. Sanyal; David Zakim.: Zakim and Boyer's Hepatology: A Textbook of Liver Disease 486. Saunders, 1990 (1990). Дата обращения: 4 сентября 2015. Архивировано 25 августа 2019 года.
- ↑ Arnold P. Appleby, Franz Müller, Serge Carpy “Weed Control“ in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. doi:10.1002/14356007.a28_165
- ↑ Pesticide Reregistration Sheet (englisch) Архивная копия от 9 декабря 1999 на Wayback Machine (PDF; 45 kB).
- ↑ Vegetable Soybean Research Needs for Production and Quality Improvement (англ.). — Taipei: Asian Vegetable Research and Development Center, 1991. — P. 89. — ISBN 9789290580478. Архивировано 7 марта 2022 года.
- ↑ Consumer Factsheet on: ALACHLOR. National Primary Drinking Water Regulations. United States Environmental Protection Agency (EPA. Дата обращения: 4 сентября 2015. Архивировано 24 сентября 2015 года.
- ↑ Cornell Herbicide Profile. Дата обращения: 27 октября 2016. Архивировано 19 июля 2016 года.
- ↑ EXTOXNET PIP - ALACHLOR. orst.edu. Дата обращения: 17 мая 2015. Архивировано 10 марта 2015 года.
- ↑ e-phy (фр.). Ministère de l'agriculture, de l'agroalimentaire. Дата обращения: 30 апреля 2013. Архивировано 1 июня 2003 года.
- ↑ Emissionsminderung für prioritäre und prioritäre gefährliche Stoffe der Wasserrahmenrichtlinie – Stoffdatenblätter – Datenblatt Alachlor Архивная копия от 12 августа 2015 на Wayback Machine, Texte 29/07, Umweltforschungsplan des Bundesministers für Umwelt, Naturschutz und Reaktorsicherheit, S. 5ff.
- ↑ Vencill, W.K. 2002. WSSA herbicide handbook (8th edition). Weed Science Society of America. Lawrence, KS, USA. ISBN 1-891276-33-6.
- ↑ Xu, J., J. W. Stucki, J. Wu, J. Kostka, and G. K. Sims. 2001. Fate of atrazine and alachlor in redox-treated ferruginous smectite. Environmental Toxicology & Chemistry 20: 2717-2724.
- ↑ Kappa, Bromide 2013. Substitutions for methane gas in high school combustion demonstrations.